
【题目】按要求书写:
(1)在H2O、NaCl、NaOH、Na2O2、H2O2中,既含有非极性键又含有极性键的是 , 既含有离子键又含有极性键的是;
(2)甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.
工业生产甲醇的常用方法是:CO(g)+2H2 (g)CH3OH(g)△H=﹣91.0kJ/mol ①
已知:2H2 (g)+O2 (g)═2H2O (l)△H=﹣572.0kJ/mol ②
H2 (g)+ ![]() O2 (g)═H2O(g)△H=﹣263.0kJ/mol ③
O2 (g)═H2O(g)△H=﹣263.0kJ/mol ③
①H2的燃烧热为 kJ/mol.
②CH3OH(g)+O2 (g)CO(g)+2H2O(g)的反应热△H=kJ/mol.
【答案】
(1)H2O2;NaOH
(2)286.0;435
【解析】解:(1)H2O是共价化合物只存在共价键;
NaCl中钠离子和氯离子之间只存在离子键;
NaOH中钠离子和氢氧根离子之间存在离子键、O原子和氢原子之间存在极性共价键;
Na2O2中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在非极性共价键;
H2O2中H原子和O原子之间只存在极性共价键,O与O原子之间为非极性键;所以答案是:H2O2;NaOH;
(2)①2H2(g)+O2(g)═2H2O(l)△H=﹣572.0kJmol﹣1①H2(g)+ ![]() O2(g)═H2O(g)△H=﹣263.0kJmol﹣1②,根据盖斯定律①×
O2(g)═H2O(g)△H=﹣263.0kJmol﹣1②,根据盖斯定律①× ![]() 可得:氢气的燃烧热的热化学方程式为:H2(g)+
可得:氢气的燃烧热的热化学方程式为:H2(g)+ ![]() O2(g)=H2O (l)△H=﹣286.0kJ/mol,所以氢气的燃烧热为:△H═﹣286.0KJ/mol,所以答案是:286.0;②CO(g)+2H2(g)CH3OH(g)△H=﹣91.0kJ/mol ①
O2(g)=H2O (l)△H=﹣286.0kJ/mol,所以氢气的燃烧热为:△H═﹣286.0KJ/mol,所以答案是:286.0;②CO(g)+2H2(g)CH3OH(g)△H=﹣91.0kJ/mol ①
H2(g)+ ![]() O2(g)=H2O(g)△H=﹣263.0kJ/mol②,根据盖斯定律②×2﹣①得到:CH3OH(g)+O2(g)CO(g)+2H2O(g)△H=﹣435 kJ/mol,所以答案是:435.
O2(g)=H2O(g)△H=﹣263.0kJ/mol②,根据盖斯定律②×2﹣①得到:CH3OH(g)+O2(g)CO(g)+2H2O(g)△H=﹣435 kJ/mol,所以答案是:435.
【考点精析】根据题目的已知条件,利用反应热和焓变的相关知识可以得到问题的答案,需要掌握在化学反应中放出或吸收的热量,通常叫反应热.


科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与应用均正确的是( )
A.SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力
B.Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒
C.氨气是一种碱性气体,可用碱石灰或无水CaCl2干燥
D.MgO的熔点很高,可用于制作耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下图所示化合物的说法不正确的是( )。

A. 既可以与Br2的CCl4溶液发生加成反应,又可以与Br2发生取代反应
B. 1mol该化合物最多可以与3molNaOH反应
C. 既可以催化加氢,又可以使酸性KMnO4溶液褪色
D. 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )。
A. 该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,其工作原理如图所示。下列关于固体燃料电池的有关说法中正确的是( )

A. 固体氧化物的作用是让电子在电池内通过
B. 固体氧化物中O2﹣从a极向b极移动
C. 电极b为电池的负极,电极反应式为:O2+4e﹣=2O2﹣
D. 若以C3H8为燃料气,则接触面上发生的反应为C3H8﹣20e﹣+10O2﹣═3CO2+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体。根据图示回答问题:
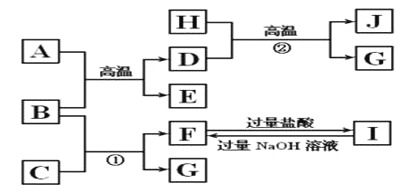
(1)写出下列物质的化学式:A________, I________,
(2)反应反应②的化学方程式是__________________;
(3)如右图所示,将I持续滴加入NaOH中开始没有沉淀生成,后来出现白色沉淀,V1:V2=_________;

(4)3molJ与足量的稀硝酸反应生成____________molNO。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3,其流程如下:

已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:FeS2 + 14Fe3+ + 8H2O =15Fe2+ + 2SO42— + 16H+
下列说法不正确的是
A. “还原”后可以用KSCN检验Fe3+是否反应完全
B. “还原”时反应Ⅱ的离子方程式为2Fe3+ + FeS2 = 2S↓+ 3Fe2+
C. “沉淀”时,可以先将溶液调节成强碱性,再加入(NH4)2CO3
D. 所得FeCO3需充分洗涤,可以用稀盐酸和BaCl2溶液检验FeCO3是否已洗涤干净
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 将铜丝插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. NaHCO3溶液中加少量Ba(OH)2溶液:HCO![]() +Ba2++OH-===BaCO3↓+H2O
+Ba2++OH-===BaCO3↓+H2O
C. 硫化钠水溶液呈碱性:S2-+2H2O===H2S↑+2OH-
D. 在酸性碘化钾溶液中滴加双氧水:2I-+2H++H2O2===I2+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com