
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、Mg2+、HCO3- | ||
| C. | NO3-、K+、[Al(OH)4]-、OH- | D. | NO3-、Mg2+、K+、Cl- |
分析 加入铝粉能放出氢气的溶液中存在大量氢离子或氢氧根离子,
A.铵根离子与氢氧根了反应,碳酸根离子与氢离子反应;
B.碳酸氢根离子与氢离子、氢氧根离子反应;
C.四种离子之间不反应,都不与氢氧根离子反应;
D.镁离子与氢氧根离子反应,硝酸根离子在酸性条件下与铝反应不会生成氢气.
解答 解:A.NH4+与氢氧根离子反应,CO32-与氢离子反应,在溶液中一定不能大量共存,故A错误;
B.HCO3-与氢离子和氢氧根离子都发生反应,在溶液中一定不能大量共存,故B错误;
C.NO3-、K+、[Al(OH)4]-、OH-之间不发生反应,都不与氢氧根离子反应,在碱性溶液中能够大量共存,故C正确;
D.Mg2+与氢氧根离子反应,在酸性条件下NO3-具有强氧化性,与Al反应不会生成氢气,在溶液中一定不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
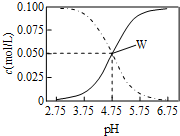 25℃时,在醋酸和醋酸钠混合溶液中有c(CH3COOH)+c(CH3COO-)=0.1mol/L且c(CH3COOH)、c(CH3COO-)与pH的关系如图.有关离子浓度叙述正确的是( )
25℃时,在醋酸和醋酸钠混合溶液中有c(CH3COOH)+c(CH3COO-)=0.1mol/L且c(CH3COOH)、c(CH3COO-)与pH的关系如图.有关离子浓度叙述正确的是( )| A. | pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol/L | |
| B. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | W点表示溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| D. | 向W点所表示溶液中通入0.05mol HCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
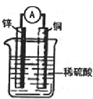 如图为某原电池示意图,请回答下列问题,
如图为某原电池示意图,请回答下列问题,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:F->Na+>Mg2+>Al3+ | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性:H2SiO3>H2CO3>H3PO4 | D. | 熔点:NaCl>SiO2>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C70与金刚石一样属于原子晶体 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | I2升华破坏了共价键 | |
| D. | HCl溶于水能电离子出H+、Cl-,所以HCl是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

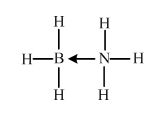 (必须标明配位犍).
(必须标明配位犍).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
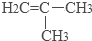 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水要现用现制,并保存在盖有橡胶塞的棕色瓶子中,置于冷暗处 | |
| B. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| C. | 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 | |
| D. | 电解NaCl溶液得到22.4 L H2(标准状况),理论上需要转移NA个电子(NA表示阿伏加德罗常数) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com