
四氯化碳是一种不溶于水且密度比水大的有机溶剂,现把溴从四氯化碳中除去,则可加入___________试液,充分振荡后,再用___________(填仪器名称)分离而得到纯净的四氯化碳,反应的化学方程式是________________________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
常温下,下列各组离子能常量共存的是 、
A.Mg2+、K+、SO42—、NO3— B.Fe2+、H+、Cl—、NO3—
C.Cu2+、Na+、OH—、Cl— D.K+、HCO3—、Ca2+、OH—
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:填空题
(6分)(1)石墨是层状结构,如下图所示。每一层内的碳原子间通过sp2杂化形成 (填代号字母,后同);层与层间存在 ;石墨的每一个碳原子经过sp2杂化后,还剩下1个未成对电子,在电场作用下能够作定向移动,因而石墨还具有导电性,所以还存在 。

a:σ键
b:π键
c:氢键
d:配位键
e:范德华力
f:金属键
g:离子键
(2)请选“>”、“<”或“=”填与下列空格中:
①熔点:Na Mg; ②硬度:金刚石 晶体硅; ③晶格能:NaI NaBr
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.H2S的电子式:
B.基态氧原子的电子排布图:
C.二氧化硅的分子式:SiO2
D.24Cr的电子排布式:[Ar]3d54s1
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:实验题
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病,KI、KIO3曾先后用于加碘盐中。
(1)工业上可以通过铁屑法生产KI,其工艺流程如下:
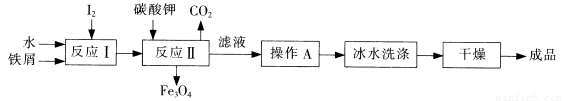
①反应I生成铁与碘的化合物(Fe3I8),若该化合物中铁元素与碘元素的质量比_______,则反应Ⅱ的化学方程式是________________________________。
②操作A包括加热浓缩、______________、______________;用冰水洗涤的目的是______________。
(2)KIO3可以通过H2O2氧化I2先制得HIO3,然后再用KOH中和的方法进行生产。
①配平第一步反应的化学方程式:___H2O2+___I2→____HIO3+____H2O
②烹饪时,含KIO3的食盐常在出锅前加入,其原因是_______________________。
③若制得1.284 kg KIO3固体,理论上至少需消耗质量分数为30%的双氧水__________kg。
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
用下列实验装置和方法进行相应实验,能达到实验目的的是

A.用图甲所示方法检查装置的气密性
B.乙图装置可用于吸收HCl气体,并防止倒吸
C.大理石和稀硫酸反应制CO2时选用丙图装置
D.用丁图所示装置将溶液定容到100mL
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
反应A+B→C分两步进行:①A+B→X;②X→C。反应过程中能量变化如图所示。下列有关叙述正确的是

A.E2表示反应X→C的反应热
B.A+B→C此反应放热
C.X是反应A+B→C的催化剂
D.加入催化剂可改变反应A+B→C的反应热
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三一模理综化学试卷(解析版) 题型:选择题
常温下,将浓度均为0.1mol/L一元酸HA溶液和NaOH溶液等体积混合,得到混合溶液①,该混合溶液pH=9,下列说法正确的是
A.①溶液中:c(A)>c(Na+)>c(OH)>c(H+)
B.①溶液中:c(HA)+c(A)=0.1mol/L
C.常温下,0.1mol/LHA溶液的pH=1
D.0.1mol/LHA溶液中:c(HA)>c(A)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三下学期初考试理综化学试卷(解析版) 题型:实验题
草酸(H2C2O4)溶液与酸性KMnO4溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为:

【提出假设】假设1: 该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是 。
【设计、完成实验】
(1)称取 g草酸晶体(H2C2O4·2H2O),配置500 mL 0.10 mol/L H2C2O4溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和 。
②下列操作会使所配溶液浓度偏低的是 (填下列选项的字母序号)。
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘
B.定容时俯视刻度线
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
(2)完成探究,记录数据
实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪[色时间[(s) | |||
0.10 mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50 mol/L 稀硫酸 | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65 ℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/L K2SO4溶液 | 18 |
则x = ,假设2成立
(3)由于KMnO4能氧化水中有机物等因素,为配制好稳定的KMnO4溶液,其浓度需标定。取10.00 mL 0.10 mol/L H2C2O4溶液于锥形瓶中,加入10 mL 0.50 mol/L稀硫酸,用(2)中KMnO4溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00 mL,则草酸溶液与酸性KMnO4溶液反应的离子方程式为: 。上述实验中KMnO4溶液的物质的量浓度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com