
常温下,下列各组离子能常量共存的是 、
A.Mg2+、K+、SO42—、NO3— B.Fe2+、H+、Cl—、NO3—
C.Cu2+、Na+、OH—、Cl— D.K+、HCO3—、Ca2+、OH—
科目:高中化学 来源:2014-2015学年江西省六校高三3月联考化学试卷(解析版) 题型:填空题
(13分)研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为____________________________。利用反应6NO2+8NH3 7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下的体积是________L。
7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下的体积是________L。
(2)已知:2SO2(g)+O2(g)  2SO3(g) ΔH=—196.6 kJ/mol ;
2SO3(g) ΔH=—196.6 kJ/mol ;
2NO(g)+O2(g)  2NO2(g) ΔH=—113.0 kJ/mol ;
2NO2(g) ΔH=—113.0 kJ/mol ;
①则反应NO2(g)+SO2(g)  SO3(g)+NO(g) ΔH 的ΔH=________。
SO3(g)+NO(g) ΔH 的ΔH=________。
②一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是___ _____。
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1 mol SO3的同时生成1 mol NO2
③测得上述反应平衡时NO2与SO2的体积比为1∶6,则平衡常数K=__ ______。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)  CH3OH(g) ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。
CH3OH(g) ΔH。CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104 kPa左右,选择此压强的理由是______________________ 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三下学期开学联考化学试卷(解析版) 题型:填空题
(6分)
某无色透明溶液可能存在Na+、Fe3+、Ba2+、NO3-、CO32-、HCO3-、SO42-中的几种离子,现有如下操作:
Ⅰ、取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ、另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
①该溶液中一定存在的离子有______________,一定不存在的离子_____________。
②用一个离子方程式表示操作②的实验现象:__________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:推断题
(B)【化学—有机化学基础】(13分)

请根据上述合成路线,回答下列问题:
(1)氢化阿托醛所含官能团的名称为 ;一定条件下,1 mol氢化阿托醛最多可跟 mol氢气加成。
(2)②的反应类型是 。
(3)写出反应③的化学方程式: 。
(4)④中所用试剂X为 。
(5)C与羧酸M在一定条件下可生成一种相对分子质量为178的酯类物质,则M的结构简式为 。
(6)氢化阿托醛具有多种同分异构体,写出符合下列特征的同分异构体的结构简式: (写出一种即可)。
①苯环上有两个取代基
②苯环上的一溴代物只有两种
③其水溶液遇FeCl3溶液呈特征颜色
④能发生加聚反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是
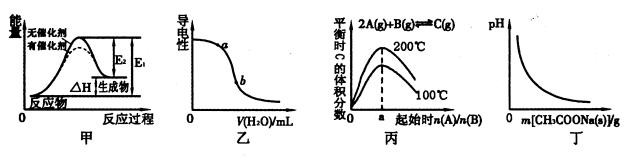
A.图甲表示催化剂能改变化学反应的焓变
B.图乙表示向氨水中加水时溶液导电性的变化情况,且溶液c(OH—)大小:a<b
C.由图丙可知反应2A(g)+B(g)  C(g)的△H >O,且 a=2
C(g)的△H >O,且 a=2
D.图丁表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化情况
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,8 g甲烷中含C-H键的数目为4NA
B.25℃时,1 L pH=13的Ba(OH) 2溶液中含有的OH—数为0.2NA
C.1 mol冰醋酸和1 mol乙醇经催化加热反应生成H2O分子数为NA
D.标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:实验题
(9分)下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:

(1)该浓盐酸的物质的量浓度为___________mol/L。
(2)某学生欲用上述浓盐酸和蒸馏水配制250 mL物质的量浓度为0.7 mol/L稀盐酸。
①该学生用量筒量取________ mL上述浓盐酸进行配制;
②所需的实验仪器有:①胶头滴管、②烧杯、③量筒、④玻璃棒,配制稀盐酸时,还缺少的仪器有 。
③下列操作导致所配制的稀盐酸的物质的量浓度偏低的是 (填字母)。
A、用量筒量取浓盐酸时俯视凹液面
B、未恢复到室温就将溶液注入容量瓶并进行定容
C、容量瓶用蒸馏水洗后未干燥
D、定容时仰视液面
E、未洗涤烧杯和玻璃棒
(3)若在标准状况下,将a L HCl气体溶于1 L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为 mol/L。
a. b.
b. c.
c. d.
d.
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
下列操作正确的是
A.有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场
B.金属钠着火时,立即用水灭火
C.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
D.用托盘天平称取5.85 g NaCl固体
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:填空题
四氯化碳是一种不溶于水且密度比水大的有机溶剂,现把溴从四氯化碳中除去,则可加入___________试液,充分振荡后,再用___________(填仪器名称)分离而得到纯净的四氯化碳,反应的化学方程式是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com