
����Ŀ��ǰ���ʿռ�վ����CO2�����漰�ķ�ӦΪCO2+4H2![]() CH4+2H2O���÷�Ӧ������˵����ȷ����
CH4+2H2O���÷�Ӧ������˵����ȷ����
A. ͨ��ʹ���ɴ�����ʹCO2 100%ת��ΪCH4
B. ���¶��£�����Ӧ��ƽ��ʱ��CH4���ʵ����Ͳ��ٱ仯����Ϊ��Ӧ��ֹͣ���ٽ���
C. ����ʹ�ô����������¶Ȼ�����ѹǿ���ܼӿ�÷�Ӧ������
D. ���������¶ȿ��Լӿ췴Ӧ���ʣ������ڹ�ҵ�����и÷�Ӧ�¶�Խ��Խ��
���𰸡�C
�������������ܹ��ı仯ѧ��Ӧ�����ʣ����Dz�Ӱ��ƽ���ƶ������ʵ�ת���ʲ��䣬A���������¶��£�����Ӧ��ƽ��ʱ��CH4���ʵ����Ͳ��ٱ仯����Ӧ�ﵽƽ��״̬����ʱ��V(��)= V(��)��0��Ϊ��̬ƽ�⣬����ֹͣ��B�����������¶ȣ�����������ٷ��������ӣ����ʼӿ죬����ѹǿ����С�����������Ũ������Ӧ���ʼӿ죬C��ȷ�������¶ȿ��Լӿ췴Ӧ���ʣ����Ƕ��ڷ��ȷ�Ӧ��˵���¶�̫�ߣ�ƽ�����ƣ������ڲ�������ɣ������ڹ�ҵ�����в��Ǹ÷�Ӧ�¶�Խ��Խ�ã�D��������ȷѡ��C��
�㾦; ���ڿ���÷�Ӧ��˵��ʹ�ô�����ֻ�ܸı䷴Ӧ����������ƽ����ƶ���Ӱ������˷�Ӧ���ת���ʲ������仯��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪�ú��������ķ�Һ(����������)���Ʊ�Ħ���Σ���(NH4)2Fe(SO4)2��6H2O��������������£�

�ش��������⣺
���Լ�X��_______��д����������Ҫ��Ӧ�����ӷ���ʽ___________��
�ڲ����������Ϊ��________��_________��
��Ϊ�ⶨ(NH4)2Fe(SO4)2��6H2O���������ĺ�����ijʵ��С����������ʵ�飺�õ�����ƽȷ����5.000g��������茶��壬���Ƴ�250mL��Һ��ȡ������Һ25.00mL����ƿ�У���ϡH2SO4�ữ����0.01000mol/LKMnO4��Һ�ζ����������KMnO4��Һ��ƽ�����Ϊ22.00mL��
�ζ��յ������Ϊ�� _______________________���þ�����������������Ϊ___________��������4λ��Ч���֣�
��2��ij������ͨ��ʵ�����Ħ���ξ������ʱ�ķֽ���
��Ħ�������ȷֽ⣬С��ͬѧ��Ϊ�ֽ������������¼��������
a��Fe2O3��SO3��NH3��H2O b��FeO��NH3��SO3��H2O
c��FeO��SO2��NH3��H2Od��Fe2O3��NH3��SO2��SO3��H2O
�����������ͨ����������ȷ��������___________������������ţ���
����ͬѧ�������ͼװ�ã�����Aװ���еĹ����Ϊ����ɫ�����������к���_____________��Cװ���к�ɫ��ȥ��˵����������к���__________��Cװ�ú�Ӧ����β������װ��D��D��ʢ�е��Լ�������__________(дһ�ּ���)��

�۱�ͬѧ����������װ��֤���ֽ�����к��а�����ֻ�����B��C�е��Լ����ɣ����������Լ�ΪB______________��C______________��
�ܶ�ͬѧ��ΪĦ���ηֽ���ܻ�����N2��SO3���������װ����ѡ���Ҫ��װ�ü���֤��������ȷ������˳�������������A��______________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���X��һ����Ҫ���л�����ԭ�ϣ���ͼ��ʾ�����л���XΪԭ����Ƶĺϳ�·��(���ֲ������ϳ�·�ߡ���Ӧ��������ȥ)��

��֪����.XΪ������������Է�������Ϊ92��Y��һ�ֹ��ܸ߷��Ӳ��ϡ�
��.����������Ը�����ص������£��������������Ȼ���![]() ��
��
��. ![]() (�������ױ�����)��
(�������ױ�����)��
����ݱ���������Ϣ����ѧ֪ʶ�ش��������⣺
(1)X�ṹ��ʽΪ________________��![]() �й����ŵ�����Ϊ______________��
�й����ŵ�����Ϊ______________��
(2)��Ӧ�۵ķ�Ӧ������__________����Ӧ�ں͢۵�˳���ܽ�����ԭ����_____________��
(3)��֪AΪһ�ȴ��
��Ӧ�ܵĻ�ѧ����ʽΪ___________________________��
��Ӧ�ݵ����ӷ���ʽΪ_________________________��
(4)��˾ƥ���ж���ͬ���칹�壬��������������ͬ���칹����___________ �֡�
�ٷ����廯����
�ڲ��ܷ���ˮ�ⷴӦ��Ҳ���ܷ���������Ӧ��
��1mol���л����������2molNaHCO3��ȫ��Ӧ��
(5)д����AΪԭ���Ʊ�![]() �ĺϳ�·������ͼ(�����Լ���ѡ)__________���ϳ�·������ͼ��ʾ�����£�
�ĺϳ�·������ͼ(�����Լ���ѡ)__________���ϳ�·������ͼ��ʾ�����£�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1L 0.1mol��L-1NaOH��Һ����0.07molCO2��������Һ��n(Na2CO3)��n(NaHCO3)֮��ԼΪ
A. 3�U4 B. 3�U1 C. 2�U3 D. 3�U2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Na2SO3�����ֽ⣬ʵ�����̺ͽ�����£�
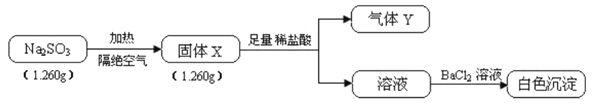
����Y��һ�ִ�����ڱ�״���µ��ܶ�Ϊ1.518g��L-1����ش�:
��1������Y���ӵĵ���ʽ___,��ɫ�����Ļ�ѧʽ_______��
��2���������е�Na2SO3���ȷֽ�Ļ�ѧ����ʽ__________��
��3����ȡ����X������Na2SO3��ϣ���ˮ�ܽ����ϡ���ᷴӦ���е���ɫ����������д����������ɫ���������ӷ���ʽ____________(�����ǿ�����Ӱ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��̽������ͭ���仯��������ʣ�ijͬѧ��Ʋ�����������ʵ�顣
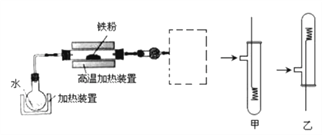
��֪: 3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)
Fe3O4(s)+4H2(g)
��ش�:
��1�� ���߿���ѡ���װ����_____ (����������������); ʵ��ʱӦ������״ͭ˿���ȣ���ں��ٳ���Ѹ���������ƵõĴ��������У��۲쵽��ʵ��������_________��
��2��ʵ���ȡӲ�ʲ������������Ĺ��壬��һ��Ũ�ȵ������ܽ⣬�μ�KSCN��Һ��û�г���Ѫ��ɫ��˵���ù�����û��+3�۵������жϽ����Ƿ���ȷ��˵������_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС������ͼ��ʾװ�òⶨ��þ�Ͻ������������������������ԭ��������
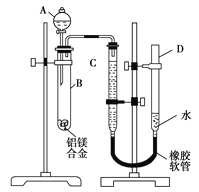
��1��A���Լ�Ϊ________��
��2��ʵ��ǰ���Ƚ���þ�Ͻ���ϡ���н���Ƭ������Ŀ����____________________��
��3���������������ҩƷ��ˮװ��������������Ӻ�װ�ú�������еIJ������У��ټ�¼C��Һ��λ�ã��ڽ�B��ʣ����������ϴ�������������أ��۴�B�в���������������ָ������º�����¼C��Һ��λ�ã�����A��B�еμ������Լ�������������˳����________(�����)����¼C��Һ��λ��ʱ����ƽ��������Ӧ________��
��4��B�з�����Ӧ�Ļ�ѧ����ʽΪ__________________________��
��5����ʵ������þ�Ͻ������Ϊa g������������Ϊb mL(�ѻ���Ϊ��״��)��B��ʣ����������Ϊc g�����������ԭ������Ϊ________��
��6��ʵ�����������δϴ�ӹ������õIJ�������������������������________(����ƫ������ƫС����������Ӱ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(Si3N4)��һ�������մɲ��ϣ�������ʯӢ�뽹̿�ڸ��µĵ�������ͨ�����·�Ӧ�Ƶã�3SiO2��6C��2N2![]() Si3N4��6CO������˵����ȷ����
Si3N4��6CO������˵����ȷ����
A. �ڵ�����ĺϳɷ�Ӧ�У������ǻ�ԭ��������������������
B. ������Ӧ��ÿ����1 mol�����裬�����õ�12 mol����
C. �÷�Ӧ�����ĸ�������Ӧ����֮һ
D. �÷�Ӧ���ж��������������Ҫβ������װ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1 L pH=10�� NaOH��Һ�г���ͨ��CO2��ͨ���CO2�������V������Һ��ˮ��������OH�� ����Ũ�ȣ������Ĺ�ϵ����ͼ��ʾ��������������ȷ���ǣ� ��

A. a����Һ�У�ˮ�������c( H+ )��1��10-10mol/L
B. b����Һ�У�c( H+ )��c( OH- )
C. c����Һ����c(OH-) > c(HCO3-)+c( H+ )
D. d����Һ�У�c(Na+)��2c(CO32-)��c(HCO3-)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com