
����Ŀ���������£����й��ڵ���ʵ�˵������ȷ����
A. �к͵��������Ũ�ȵİ�ˮ������������Һ��pH��7��ǰ�����ĵ������
B. ��NH4Cl��Һ�м���������Ũ�ȵ�ϡ���ᣬ��![]() ��ֵ��С
��ֵ��С
C. ��NaHS��Һ�м������� KOH ��c(Na��)��c(H2S)��c(HS��)��c(S2��)
D. ��a mol��L��1�Ĵ�����0.01 mol��L��1������������Һ��������(����������¶ȱ仯)��������Һ��c(Na��)��c(CH3COO��)�������ĵ��볣��Ka��![]() (�ú�a�Ĵ���ʽ��ʾ)
(�ú�a�Ĵ���ʽ��ʾ)
���𰸡�C
���������к͵��������Ũ�ȵİ�ˮ������������Һ��pH��7����ˮ���ĵ������٣���A������NH4Cl��Һ�м���������Ũ�ȵ�ϡ���ᣬ��������笠�����ˮ�⣬����![]() ��ֵ����B���������������غ㣬��NaHS��Һ�м������� KOH ��c(Na��)��c(H2S)��c(HS��)��c(S2��)����C��ȷ����a mol��L��1�Ĵ�����0.01 mol��L��1������������Һ��������(����������¶ȱ仯)��������Һ��c(Na��)��c(CH3COO��)=0.005 mol��L��1����c(CH3COOH)=
��ֵ����B���������������غ㣬��NaHS��Һ�м������� KOH ��c(Na��)��c(H2S)��c(HS��)��c(S2��)����C��ȷ����a mol��L��1�Ĵ�����0.01 mol��L��1������������Һ��������(����������¶ȱ仯)��������Һ��c(Na��)��c(CH3COO��)=0.005 mol��L��1����c(CH3COOH)= ![]() mol��L��1�������ĵ��볣��Ka��
mol��L��1�������ĵ��볣��Ka��
![]() ����D������
����D������


 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д� �ܿ���ȫ��100��ϵ�д�
�ܿ���ȫ��100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ƽ�����ʢ��ǿ��ԭ��Һ̬��(N2H4)��ǿ������Һ̬˫��ˮ�������ǻ�Ϸ�Ӧʱ������������������ˮ���������ų��������ȡ���֪0.4 molҺ̬����������Һ̬˫��ˮ��Ӧ�����ɵ�����ˮ�������ų�256 kJ��������
��1���˷�Ӧ���Ȼ�ѧ����ʽΪ_______________________________________��
��2������֪H2O(g)===H2O(l) ��H����44 kJ��mol��1��16 gҺ̬��������Һ̬˫��ˮ��Ӧ����Һ̬ˮʱ�ų�������Ϊ________kJ��
��3���˷�Ӧ���ڻ���ƽ������ͷŴ����ȺͿ��ٲ������������⣬����һ���ܴ���ŵ���________________________________��
��4���������ǿ�����̬��(N2H4)��ȼ�ϣ����������������������߷�Ӧ���ɵ�����ˮ��������֪��N2(g)��2O2(g)===2NO2(g) ��H����67.7 kJ��mol��1 N2H4(g)��O2(g)===N2(g)��2H2O(g) ��H����534 kJ��mol��1 ��̬�ºͶ���������Ӧ���Ȼ�ѧ����ʽΪ_______________________________��
��5����Ӧ2H2��O2![]() 2H2O�������仯��ͼ��ʾ��
2H2O�������仯��ͼ��ʾ��
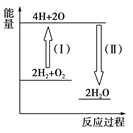
��֪��1 mol H2��1 molO2��1 mol H��O�еĻ�ѧ���ֱ���Ҫ����436 kJ��496 kJ��463 kJ����������Ӧ����(��)________(���������������ų���)________kJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��X��Y��Q��W ���Ƕ��Ե缫������Դ��ͨ��W��������ɫ�������˵���д�����ǣ� �� 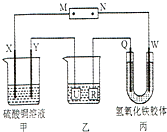
A.��Դ��M��Ϊ����
B.��װ������Һ��pH��С
C.��װ�õ������缫�϶��е������������ʵ���֮��Ϊ1��1
D.������װ�ø�ͭ������U��Ӧ����Ag�����Һѡ��AgNO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л������������˵����ȷ����
A.���͵����ʶ��Ǹ߷��ӻ����ˮ�������ͬ
B.������ϩ����ʹ��ˮ��ɫ��������ˮ�����ӳɷ�Ӧ
C.������������֬��Ϊͬϵ��
D.������Ҵ����ܷ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Һ�絼��Խ������Խǿ����������0.100 mol��L��1����ֱ�ζ�10.00 mLŨ�Ⱦ�Ϊ0.100 mol��L��1��NaOH��Һ�Ͷ��װ�[(CH3)2NH]��Һ (���װ���ˮ�еĵ����백���ƣ��ڳ�����Kb[(CH3)2NH��H2O]��1.6��10��4 )�����ô�������õζ���������Һ�ĵ絼����ͼ��ʾ������˵����ȷ����
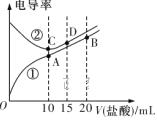
A. D����Һ�У�2c(Na��)��3c(Cl��)
B. A����Һ�У�c(H��)��c(OH��)��c[(CH3)2NH��H2O]
C. ���ߢڴ����ζ����װ���Һ������
D. ����ͬ�¶��£�A��B��C��D�ĵ����Һ�У�ˮ�ĵ���̶�������C��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���10 mL 0.40 mol��L��1 H2O2��Һ�м�������FeCl3��Һ����ͬʱ�̲������O2�����(������Ϊ��״��)���±���ʾ��
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
������ʾ����Ӧ���������У��� 2Fe3+��H2O2 == 2Fe2+��O2����2H+���� H2O2��2Fe2+��2H+ == 2H2O��2Fe3+����Ӧ�����������仯����ͼ��ʾ������˵���������
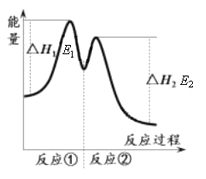
A. Fe3+�������������������ķֽ�����
B. ��Ӧ�������ȷ�Ӧ����Ӧ���Ƿ��ȷ�Ӧ
C. ��Ӧ2H2O2(aq) == 2H2O(l)��O2(g)����H��E1��E2��0
D. 0��6 min��ƽ����Ӧ���ʣ�v(H2O2)��3.33��10��2 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѡ����˵������ʽΪC4H6��ij����![]() ��������CH2=CH-CH=CH2����ʵ��
��������CH2=CH-CH=CH2����ʵ��
A. ȼ����Ũ��
B. ��ʹ���Ը��������Һ��ɫ
C. ��������ˮ��Ӧ����������ֻ��2��̼ԭ��������ԭ��
D. �����������ʵ���֮��1��2��Ӧֻ��1�ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ���У�����þ�����͵�����ͨ������������ 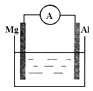
��1�����ձ�����ҺΪϡ���ᣬ�����ĵ缫��ӦʽΪ�� ������
���� ��
��2�����ձ�����ҺΪ����������Һ�������ĵ缫��ӦʽΪ�� ������
���� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com