
【题目】能够充分说明在恒温下的密闭容器中,反应2SO2+O2![]() 2SO3已达平衡状态的标志是
2SO3已达平衡状态的标志是
A. 容器中SO2.O2.SO3的物质的量之比为2:1:2
B. SO2 和SO3的物质的量浓度相等
C. 单位时间内生成2molSO3 时,即消耗1molO2
D. 反应容器内压强不随时间变化而变化
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.含有羟基的化合物一定属于醇类
B.代表醇类的官能团是与烃基或苯环侧链上的碳原子相连的羟基
C.酚类和醇类具有相同的官能团,因而具有相同的化学性质
D.分子内有苯环和羟基的化合物一定是酚类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.1mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个Cl2分子的质量为35.5g
D.标准状况下,1mol任何物质的体积均约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存的是
A.Fe3+、Cu2+、Cl-、NO3—B.H+、Na+、AlO2—、CO32—
C.Ca2+、Fe2+、SO42—、ClO-D.Mg2+、NH4+、OH-、HCO3—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废旧镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO。制备流程图如下:
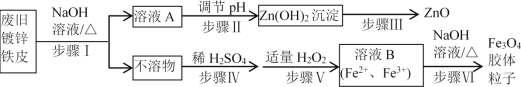
已知:Zn及化合物的性质与Al及化合物的性质相似。请回答下列问题:
(1)步骤Ⅰ用NaOH溶液处理废旧镀锌铁皮的作用有________。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)步骤Ⅲ的实验操作是______________________。
(3)写出步骤Ⅳ反应的化学方程式_______________。写出步骤Ⅴ反应的离子方程式__________。
(4)Fe3O4胶体粒子能否用过滤法实现固液分离?____(填“能”或“不能”),理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 胶体属于纯净物
B. 可用丁达尔效应区分胶体与溶液
C. 氢氧化铁胶体能吸附水中的悬浮颗粒并沉降而用于净水
D. 胶体分散质粒子的直径在10-9~10-7m之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是( )
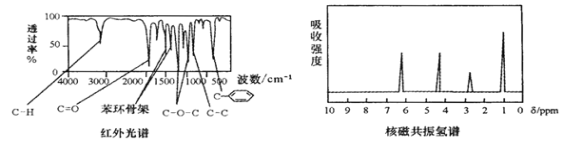
A. 由红外光谱可知,A中含有C-H键、C=O键、![]() 等
等
B. 由核磁共振氢谱可知,该有机物分子中有4种不同化学环境的氢原子
C. 若A的化学式为C8H8O2,则其结构简式可能为![]()
D. 由以上信息可以推测A分子可能为含有酯基的芳香族化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固定容积为2L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
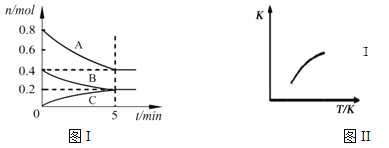
A. 该反应可表示为:2A(g)+B(g)![]() C(g)ΔH﹤0
C(g)ΔH﹤0
B. t℃时该反应的平衡常数K=6.25
C. 当容器中气体密度不再变化时,该反应达到平衡状态
D. t℃,在第6 min时再向体系中充入0.4 mol C,再次达到平衡时C的体积分数大于0.25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com