
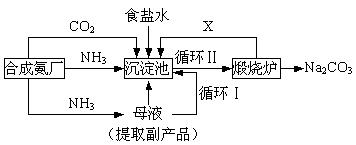

 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源:不详 题型:实验题
| A.汽油 | B.酒精 | C.苯 | D.水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
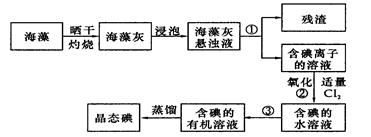
| A.苯、酒精 | B.四氯化碳、苯 | C.汽油、醋酸 | D.汽油、氨水 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
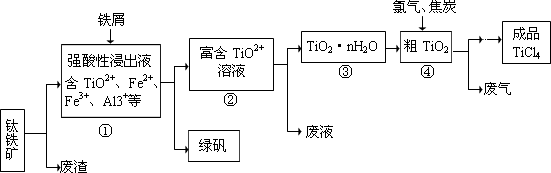
| | TiCl4 | SiCl4 |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在电解铝工业中添加冰晶石 |
| B.研制出性能优良的催化剂,降低反应所需温度 |
| C.开发太阳能、风能、氢能等清洁能源 |
| D.大力发展火电,缓解用电紧张 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.人类利用的能源都是通过化学反应获得的 |
| B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| C.物质的化学能可以在不同条件下转为热能、电能为人类所利用 |
| D.化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
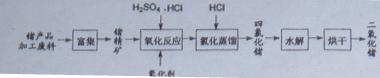
 2O2反应生成Ge4+,写出该反应的离子方程式 。
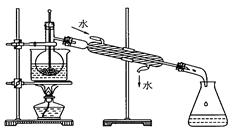
2O2反应生成Ge4+,写出该反应的离子方程式 。 (2)蒸馏可获得沸点较低的GeCl4,在此过程中加入浓盐酸的原因是 。实验室蒸馏操作时常用的玻璃仪器有:酒精灯、蒸馏烧瓶、 、 、接收管、锥形瓶等。
(2)蒸馏可获得沸点较低的GeCl4,在此过程中加入浓盐酸的原因是 。实验室蒸馏操作时常用的玻璃仪器有:酒精灯、蒸馏烧瓶、 、 、接收管、锥形瓶等。 。
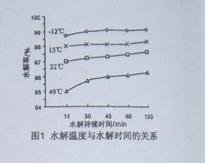
。

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④⑤ | B.②③⑥⑦ | C.③⑥⑦⑧ | D.①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com