
下列关于氯的说法正确的是( )
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B. Cl、
Cl、 Cl为不同的核素,有不同的化学性质
Cl为不同的核素,有不同的化学性质
C.实验室制备Cl2可用排饱和食盐水集气法收集
D.1.12 L Cl2含有1.7NA个质子(NA表示阿伏加德罗常数)
科目:高中化学 来源: 题型:
分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是
| “神十” 发射 火箭 燃料 | 液氢 (H2) | ①2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1 ②2H2(l)+O2(l)===2H2O(g) ΔH=-482.6 kJ·mol-1 |
| 奥运会 火炬 燃料 | 丙烷 (C3H8) | ③C3H8(l)+5O2(g)===3CO2(g)+4H2O(g) ΔH=-2 013.8 kJ·mol-1 ④C3H8(g |
A.571.6 kJ·mol-1,2 221.5 kJ·mol-1
B.241.3 kJ·mol-1,2 013.8 kJ·mol-1
C.285.8 kJ·mol-1,2 013.8 kJ·mol-1
D.285.8 kJ·mol-1,2 221.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.用金属钠可区分乙醇和乙醚
B.用高锰酸钾酸性溶液可区分己烷和3己烯
C.用水可区分苯和溴苯
D.用新制的银氨溶液可区分甲酸甲酯和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
美国化学家R.F.Heck因发现如下Heck反应而获得2010年诺贝尔化学奖。
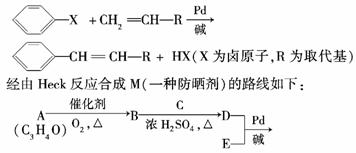
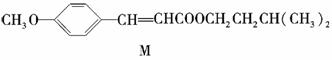
回答下列问题:
(1)M可发生的反应类型是________。
a.取代反应 b.酯化反应
c.缩聚反应 d.加成反应
(2)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式是________________________________________________________________________。
D在一定条件下反应生成高分子化合物G,G的结构简式是_____________________。
(3)在A→B的反应中,检验A是否反应完全的试剂是________。
(4)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同 化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为___________________________________________________________________。
化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为___________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
解析:(1)利用“N”守恒可知需m(NaN3)= ×
×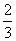 ×65 g·mol-1=78 g。
×65 g·mol-1=78 g。
(2)①由反应方程式可知产生1 mol H2同时生产2 mol OH-,故c(OH-)=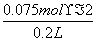 =0.75 mol/L;②设合金中Na、K的物质的量分别为a mol、b mol,然后利用质量守恒与得失电子守恒可得方程式:a+b=0.75×2和23a+39b=5.05,解得a=0.050 mol、b=0.10 mol,故可得到合金的化学式为NaK2。
=0.75 mol/L;②设合金中Na、K的物质的量分别为a mol、b mol,然后利用质量守恒与得失电子守恒可得方程式:a+b=0.75×2和23a+39b=5.05,解得a=0.050 mol、b=0.10 mol,故可得到合金的化学式为NaK2。
(3)若溶液仅含NaAl(OH)4,利用方程式可知得到24 mol Al(OH)3的同时生成12 mol Na2CO3,而实际得到24 mol Al(OH)3 与15 mol Na2CO3,说明溶液中含有NaOH,且NaOH优先与CO2反应生成Na2CO3,利用Na守恒知溶液中n(NaOH)=(15-12) mol×2=6 mol,故通入 112 L (5 mol)CO2先与NaOH作用消耗3 mol CO2生成3 mol Na2CO3,然后2 mol CO2与NaAl(OH)4作用得到4 mol Al(OH)3和2 mol Na2CO3,故n[Al(OH)3]∶n(Na2CO3)=4∶(3+2)=4∶5。
(4)由NaOH+HCl===NaCl+H2O可知溶液pH=7时,二者恰好反应完全,故三次实验得到的固体均为纯净氯化钠,利用“钠守恒”得 =
=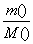 ,利用该式和题中数据可计算出三次实验中所取氢氧化钠样品的摩尔质量,进而可得出结论。
,利用该式和题中数据可计算出三次实验中所取氢氧化钠样品的摩尔质量,进而可得出结论。
答案:(1)78 (2)①c(OH-)=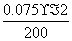 ×1 000=0.75 (mol/L)
×1 000=0.75 (mol/L)
②设上述合金中含a mol钠、b mol钾,则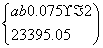
a=0.050 b=0.10
该钠—钾合金的化学式为NaK2。
(3)溶液含氢氧化钠。氢氧化钠和二氧化碳反应生成碳酸钠:15-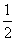 ×24=3 (mol)
×24=3 (mol)
112 L二氧化碳的物质的量: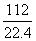 =5 (mol)
=5 (mol)
n[Al(OH)3]∶(Na2CO3)=[(5-3)×2]∶5=4∶5
(4)由氯化钠的质量推算,氢氧化钠样品的摩尔质量为
M1(氢氧化钠)= ×2.40=40 (g/mol)
×2.40=40 (g/mol)
M2(氢氧化钠)=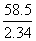 ×2.32=58 (g/mol)
×2.32=58 (g/mol)
M3(氢氧化钠)= ×3.48=58 (g/mol)
×3.48=58 (g/mol)
结论:
实验①所取氢氧化钠样品是NaOH;
实验②和实验③所取氢氧化钠样品应该是NaOH·H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
请回答下列实验室中制取气体的有关问题.
(1)如图是用KMnO4与浓盐酸反应制取适量氯气的简易装置.

装置B、C、D的作用分别是:
B________________________________________________________________________;
C________________________________________________________________________;
D________________________________________________________________________.
(2)在实验室欲制取适量NO气体.
①下图中最适合完成该实验的简易装置是________(填序号);
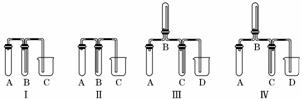
②根据所选的装置完成下表(不需要的可不填):
| 应加入的物质 | 所起的作用 | |
| A | ||
| B | ||
| C | ||
| D |
③简单描述应观察到的实验现象_________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
在水溶液中能大量共存,且加入过量稀硫酸时,有气体生成的是( )
A. Na+、Ag+、CO32-、Cl- B. K+、 Ba2+、 SO42-、Cl-
C. Na+、K+、CO32-、Cl- D. Na+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇燃料电池工作原理如下图,下列说法不正确的是
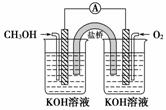
A.盐桥中的K+向负极移动
B.负极电极反应方程式为:
CH3OH-6e-+8OH-===CO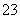 +6H2O
+6H2O
C.每消耗1 mol甲醇,需消耗33.6 L标况下的氧气
D.正极烧杯中溶液pH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com