
| ||
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(15分)【化学与技术】
氯碱工业中曾用石棉隔膜电解槽来电解食盐水,下图即为石棉隔膜电解槽的示意图,回答下列问题:
(1)产物A是 ;产物B是 ;产物C
(2)石棉隔膜能阻止 不能通过,但不能阻止 通过。
(3)粗盐水含Ca2+、Mg2+、SO42-等杂质离子,这些离子的存在除了会影响电解所得产品的纯度外,主要会 所以电解食盐水要求对粗盐水进行精制,请将精制时除去上述三种离子通常加入的化学试剂按加入的顺序依次写来 , 形成沉淀过滤后,还应加入盐酸调节pH,过滤所需要的玻璃仪器有
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省平顶山市高一上学期期末调研考试化学试卷(带解析) 题型:问答题
【化学—选修2:化学与技术】(15分) 请回答氯碱工业的如下问题:
请回答氯碱工业的如下问题: (1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果);
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果); (2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号)
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号) (3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
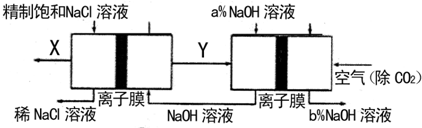
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。 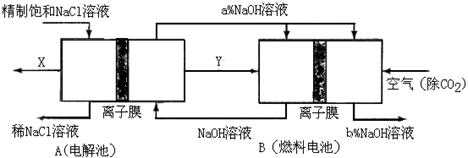
 ①图中X是__ ___(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
①图中X是__ ___(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________; ②分别写出燃料电池B中正极、负极上发生的电极反应正极:______; 负极:_____;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______; 负极:_____; ③这样设计的主要节(电)能之处在于(写出2处)____________、____________。
③这样设计的主要节(电)能之处在于(写出2处)____________、____________。
查看答案和解析>>
科目:高中化学 来源:2010届陕西留坝中学高三模拟考试化学卷 题型:填空题
(15分)【化学与技术】
氯碱工业中曾用石棉隔膜电解槽来电解食盐水,下图即为石棉隔膜电解槽的示意图,回答下列问题:
(1)产物A是 ;产物B是 ;产物C
(2)石棉隔膜能阻止 不能通过,但不能阻止 通过。
(3)粗盐水含Ca2+、Mg2+、SO42-等杂质离子,这些离子的存在除了会影响电解所得产品的纯度外,主要会 所以电解食盐水要求对粗盐水进行精制,请将精制时除去上述三种离子通常加入的化学试剂按加入的顺序依次写来 , 形成沉淀过滤后,还应加入盐酸调节pH,过滤所需要的玻璃仪器有
查看答案和解析>>
科目:高中化学 来源:2014届河南省平顶山市高一上学期期末调研考试化学试卷(解析版) 题型:简答题
【化学—选修2:化学与技术】(15分)
请回答氯碱工业的如下问题:
 (1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果);
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号)
 (3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。

①图中X是__ ___(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
 ②分别写出燃料电池B中正极、负极上发生的电极反应正极:______; 负极:_____;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______; 负极:_____;
③这样设计的主要节(电)能之处在于(写出2处)____________、____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com