
����Ŀ����֪���屽���۵�Ϊ30.8�棬�е�156�档ʵ�����ñ���Һ����ȡ�屽��װ����ͼ��
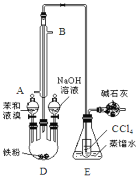
��1�������ܵ�����___��
��2��E��С�Թ���CCl4����___��
��3����ʵ��֤����ȡ�屽�ķ�Ӧ��ȡ����Ӧ�������ӵ��Լ���___��
��4��д��ͼ��װ�м�ʯ�ҵ�����������___��
��5�������廹���ܷ�������Ӧ���ɶԶ��屽���е�220�棩���ڶ��屽���е�224�棩����ʵ��õ����屽�л����ж��屽����ͨ��___������뷽�����ᴿ�õ��屽��д�����ɶԶ��屽�Ļ�ѧ����ʽ___��
���𰸡����������浼�� ����HBr�л��е�Br2����������� ��������Һ������������Һ��ϡ���ᣩ ���θ���� ������� ![]() +2Br2
+2Br2![]()
![]() +2HBr
+2HBr
��������
��ʵ��װ�ÿ�֪��������ƿ��Fe���巴Ӧ�����廯���������巢��ȡ����Ӧ�����屽���廯�⣬����AΪ�����ܣ�������������Ӧ�ʹ��Ӧ���ַ�Ӧ��NaOH��Һ����ȥ��ʣ����嵥�ʣ���ƿ��С�Թ��е�CCl4���Է�ֹ�����������ջӷ����壬�ݴ˴��⡣
(1)��Ӧ���������ڱ���Һ�巴Ӧ���ȣ�ʹ��Ӧ��������ȥ�����²��ʽϵͣ��ڷ�Ӧװ��������һ�������ܿ���ʹ�������ķ�Ӧ��Һ�����ط�Ӧװ���У��ʴ�Ϊ�����������浼����
(2)�������ӷ�������Ϊ�˳�ȥ�廯���м������ĵ����壬��Ҫ���Ȼ�̼��ͬʱ�����廯�ⲻ����CCl4�����װ�û��������ڷ�ֹ�������ʴ�Ϊ������HBr�л��е�Br2�������������
(3)�������ȡ����Ӧ����һ�������廯�⣬��˿���ͨ����������������֤���Լ�����������Һ��
(4)ͼ��װ�м�ʯ�ҵ����������θ���ܣ�
(5)�����屽�Ͷ��屽�ķе������Բ��죬�ʿ�����������ķ������屽�Ͷ��屽�ֿ������ɶԶ��屽�ķ���ʽΪ![]() +2Br2
+2Br2![]()
![]() +2HBr��
+2HBr��


 ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�������A�����ϣ��������к�̼Ϊ70.59%������Ϊ 5.88%�����ຬ�������������з����ⶨ���л����������Է��������ͷ��ӽṹ��
����һ��������������֪A��������ͼ��
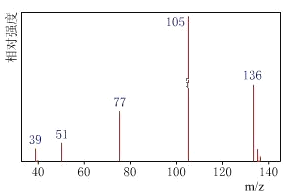
���������˴Ź����Dz��A�ĺ˴Ź���������4���壬�����֮��Ϊ1��2��2��3��
�����������ú�������Dz��A���ӵĺ�����ף���ͼ��
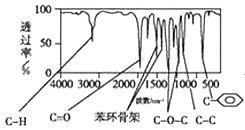
��1�������й���____�ֻ�ѧ������ͬ����ԭ�ӡ�
��2��A�ķ���ʽΪ____��
��3��������������һ���л���____��
��4��A�ķ�����ֻ��һ������������____(�����)��
a A����Է������� b A�ķ���ʽ
c A�ĺ˴Ź�������ͼ d A���ӵĺ������ͼ
��5��A�Ľṹ��ʽΪ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�������Ա�������CO2��CH4ת��Ϊ�߸���ֵ��ƷCH3COOH�Ĵ���Ӧ���̡�������ʾ��ͼ���¡�

����˵������ȷ����
A. ����CH3COOH�ܷ�Ӧ��ԭ��������Ϊ100%
B. CH4��CH3COOH����������C�DH����������
C. �١����ų��������γ���C�DC��
D. �ô�������Ч��߷�Ӧ���ƽ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Լռ����������71%����ˮ��ѧ��Դ�����þ��зdz�������ǰ����
��1����ˮɹ�οɻ�ô��Σ���ʵ�����д��ξ����ܽ⡢________��________���Ƶþ��Ρ��������������ƣ�
��2��þ����Ͻ���һ����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ģ�����Ҫ�������£�
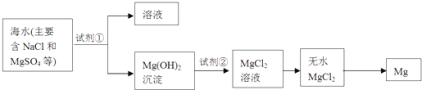
��Ϊ��ʹMgSO4ת��ΪMg��OH��2 �� �Լ��ٿ���ѡ��________��
���Դӽ�Լ��Դ����߽���þ�Ĵ��ȷ������������˵�ұþ������________��
A��Mg��OH��![]() MgO
MgO![]() Mg B��Mg��OH��
Mg B��Mg��OH��![]() MgO
MgO![]() Mg
Mg
C��Mg��OH��2![]() MgCl2
MgCl2![]() Mg D��Mg��OH��2
Mg D��Mg��OH��2![]() MgCl2
MgCl2![]() Mg
Mg
��3���弰�仯������;ʮ�ֹ㷺���ҹ����ڴ�����չ��ˮ������о��Ϳ�����������ҵ��Ũ����ˮΪԭ����ȡ��IJ��ֹ������£�
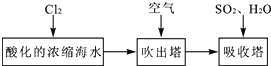
ij����С����ʵ����ģ�����������������װ�ý���ʵ�飨��������Ʒ���ѱ��������г�װ������ȥ����
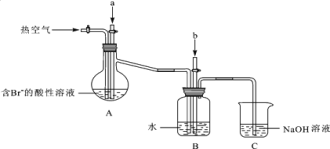
��Aװ����ͨ��a�����Ŀ���ǣ������ӷ���ʽ��ʾ��______________________________��
��Aװ����ͨ��a����һ��ʱ���ֹͣͨ�룬��ͨ�ȿ�����ͨ���ȿ�����Ŀ����___________��
�۷�Ӧ�����У�Bװ������SO42�����ɣ�����SO42���ķ�����____________________________��
��Cװ�õ�������______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β���к���CO��NO���к����塣
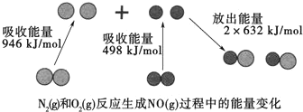
��1������β����NO���ɹ��̵������仯��ͼʾ��1molN2��1molO2��ȫ��Ӧ����NO��________�����������������ų�����________kJ������
��2��һ�����ʹ�������NO��CO�ķ�Ӧ��2NO+2CO![]() 2CO2+N2����֪��������ıȱ��������߸÷�Ӧ���ʣ�Ϊ����֤�¶ȡ������ıȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬���������Ѿ����ڱ��С�
2CO2+N2����֪��������ıȱ��������߸÷�Ӧ���ʣ�Ϊ����֤�¶ȡ������ıȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬���������Ѿ����ڱ��С�
ʵ���� | t������ | NO��ʼŨ�� ��mol/L�� | CO��ʼŨ�ȣ�mol/L�� | �����ıȱ������m2/g�� |
�� | 280 | 1.2��10-3 | 5.80��10-3 | 82 |
�� | 280 | 1.2��10-3 | b | 124 |
�� | 350 | a | 5.80��10-3 | 82 |
���뽫�������ݲ���������a___________��
������֤�¶ȶԻ�ѧ��Ӧ���ʹ��ɵ���ʵ��____________________����ʵ����ţ���
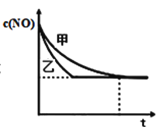
��ʵ������ʵ�����У�NO�����ʵ���Ũ��c��NO����ʱ��t�ı仯������ͼ��ʾ�����б�ʾʵ������������________________����������������������
�����ݻ��̶��������з�����Ӧ2NO+2CO![]() 2CO2+N2������˵���Ѵﵽƽ��״̬����________��������ѡ��
2CO2+N2������˵���Ѵﵽƽ��״̬����________��������ѡ��
A��������COŨ�Ȳ��� B��������NO��Ũ�ȵ���CO2��Ũ��
C��v��(NO)=2v��(N2) D�������ڻ�������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ��ѡ��3�����ʽṹ������]��15�֣�A��B��C��DΪԭ�������������������Ԫ����A2-��B+������ͬ�ĵ��ӹ��ͣ�C�� DΪͬ����Ԫ����C�������������������������3����DԪ���������һ��δ�ɶԵ��ӡ��ش��������⣺
��1������Ԫ���е縺�������� ����Ԫ�ط��ţ�������Cԭ�ӵĺ�������Ų�ʽΪ__________��
��2������A������ͬ�������壬���зе�ߵ��� �������ʽ����ԭ���� ��A��B���⻯�������ľ������ͷֱ�Ϊ �� ��
��3��C��D��Ӧ��������ɱ�Ϊ1��3�Ļ�����E�� E�����幹��Ϊ ������ԭ�ӵ��ӻ��������Ϊ ��
��4��������D2A�����幹��Ϊ ������ԭ�ӵļ۲���Ӷ���Ϊ ������D��ʪ���Na2CO3��Ӧ���Ʊ�D2A���仯ѧ����ʽΪ ��
��5��A��B�ܹ��γɻ�����F���侧���ṹ��ͼ��ʾ������������a��0.566nm�� F �Ļ�ѧʽΪ ��������A ԭ�ӵ���λ��Ϊ ����ʽ���㾧��F���ܶȣ�g.cm-3�� ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��W��ԭ������������������ԭ�ӵ�����������֮��Ϊ14��Z�Ƕ���������Ԫ����ԭ�Ӱ뾶����Ԫ�أ�Z��Xԭ�ӵ�������������ͬ��Y��Wͬ���塣����˵����ȷ���ǣ� ��
A.X��Yֻ���γ�һ�ֻ�����
B.ԭ�Ӱ뾶��r(Y)��r(W)��r(Z)
C.W�ļ���̬�⻯������ȶ��Ա�Y��ǿ
D.Z������������Ӧ��ˮ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʮ���Աʹ�õ�����ƿ���Ծ���������Ϊԭ�ϡ��ס��ҡ������������Ǻϳɾ��������ֵĻ���ԭ�ϡ�����˵������ȷ���ǣ� ��
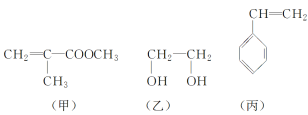
A.��������һ�������¿��������л��߷��ӻ�����
B.1mol�����ʿ���2mol����ȫ��Ӧ����2mol����
C.�ס��ҡ������ʶ��ܹ�ʹ������Ȼ�̼��Һ��ɫ
D.������ʹ���Ը��������Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ��е�λ����ͼ��ʾ����Yԭ�ӵ������������Ǵ�����������3��������˵������ȷ����( )

A.ԭ�Ӱ뾶��W��Z��Y��X
B.����������Ӧˮ��������ԣ�Z��W��X
C.����Ԫ�صĵ����У�Z���ʵ��ۡ��е����
D.W�ĵ�������ˮ��Ӧ������һ�־���Ư���Ե�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com