
 为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验: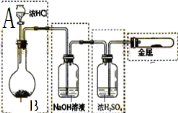


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
![]() 实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
![]() 实验二:取上述实验一后锥形瓶中清液,进行如下实验:
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
![]() (1)该清液滴在有色布条上有极强的漂白作用。(2)该清液中滴加碳酸钠溶液产生白色沉淀。(3)该清液中滴加盐酸可产生大量气体。(4)该清液加热后变浑浊并产生大量气体。
(1)该清液滴在有色布条上有极强的漂白作用。(2)该清液中滴加碳酸钠溶液产生白色沉淀。(3)该清液中滴加盐酸可产生大量气体。(4)该清液加热后变浑浊并产生大量气体。
![]()
 实验三:该学生设想用下列装置收集实验二中产生的气体作进一步检验。
实验三:该学生设想用下列装置收集实验二中产生的气体作进一步检验。
![]() 回答下列问题:
回答下列问题:
![]() (1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有 (写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有 离子;清液中滴加盐酸产生的气体是 ;清液加热后产生浑浊的原因是因为生成了 物质。
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有 (写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有 离子;清液中滴加盐酸产生的气体是 ;清液加热后产生浑浊的原因是因为生成了 物质。
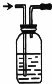
![]() (2)实验三中,洗气装置内的洗涤液一般用 溶液。
(2)实验三中,洗气装置内的洗涤液一般用 溶液。
![]() (3)在反应物的量相同情况下,该学生尝试用集气装置A和集气装置B分别和洗气装置相连来收集气体。选用集气装置 (选填“A”或“B”)可收集到更多的气体。经试验,该学生最终选用集气装置B进行下一步实验。其选择装置B的原因是
(3)在反应物的量相同情况下,该学生尝试用集气装置A和集气装置B分别和洗气装置相连来收集气体。选用集气装置 (选填“A”或“B”)可收集到更多的气体。经试验,该学生最终选用集气装置B进行下一步实验。其选择装置B的原因是
![]() 。
。
![]() (4)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为 。
(4)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2013届山东省泰安市宁阳二中高三第一次月考化学试卷(带解析) 题型:实验题
(6分)为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用。②该清液中滴加碳酸钠溶液产生白色沉淀。③该清液中滴加盐酸可产生大量气体。④该清液加热后变浑浊并产生大量气体。
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有_________(写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有______离子;清液中滴加盐酸产生的气体是________;清液加热后产生浑浊的原因是因为生成了________。
(2)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为:
。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省泰安市高三第一次月考化学试卷(解析版) 题型:选择题
为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用。②该清液中滴加碳酸钠溶液产生白色沉淀。③该清液中滴加盐酸可产生大量气体。④该清液加热后变浑浊并产生大量气体。
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有______________(写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有______离子;清液中滴加盐酸产生的气体是________;清液加热后产生浑浊的原因是因为生成了________。
(2)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为:
。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省泰安市高三第一次月考化学试卷(解析版) 题型:实验题
(6分)为了研究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生少量气体。
实验二:取上述实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用。②该清液中滴加碳酸钠溶液产生白色沉淀。③该清液中滴加盐酸可产生大量气体。④该清液加热后变浑浊并产生大量气体。
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有_________(写化学式);清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有______离子;清液中滴加盐酸产生的气体是________;清液加热后产生浑浊的原因是因为生成了________。
(2)该学生通过上述实验,写出氯水和碳酸钙反应的化学方程式为:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com