
【题目】2013年9月,中国华北华中地区发生了严重的雾霾天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染。汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霾形成的原因。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0,在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1 时刻达到平衡状态。
N2(g)+2CO2(g) △H<0,在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1 时刻达到平衡状态。
①能判断该反应达到平衡状态的标志是____________________。
A.在单位时间内生成1mol CO2的同时消耗了1mol CO B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.混合气体的压强不再变化
②在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件。请在右图中补充画出从t2 到t4 时刻正反应速率随时间的变化曲线:_____________
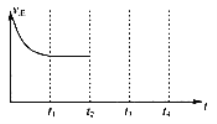
(2)改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气,1.2g 碳完全反应,吸收热量13.13kJ.
①该反应的热化学方程式为______________________________________________
②煤气化过程中产生的有害气体H2S可用足量的Na2C03溶液吸收,该反应的离子方程式为___________________________________________________。(已知:H2S: ![]() ;
; ![]() ;H2CO3:
;H2CO3: ![]() ;
; ![]() )
)
(3)已知反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
CO | H2O | H2 | CO | 0 | ||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验1条件下平衡常数K=______________(保留小数点后二位)。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是__________。
③该反应的△H ______0(填“<”或“>”);若在900℃时,另做一组实验,在此容器中加入l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2,则此时v正___________v逆(填“<”,“>”,“=”)。
【答案】 CD 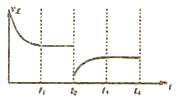 C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3kJ·mol-1 H2S+CO32-=HCO3-+HS- 2.67 a<b < >
C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3kJ·mol-1 H2S+CO32-=HCO3-+HS- 2.67 a<b < >
【解析】(1)①A.在单位时间内生成1mol CO2的同时消耗了1mol CO,从反应开始到平衡,都符合这等量关系,故A不选;B.混合气体的密度不再改变,体积不变,反应体系都是气体,从反应开始到平衡,密度始终不变,故B不选;C.混合气体的平均相对分子质量不再改变,说明各物质的物质的量不变,达平衡状态,故C选;D:混合气体的压强不再变化,说明各物质的物质的量不变,达平衡状态,故D选;故答案为:CD;
②将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,相当于减小压强,正逆反应速率都比原来的小,平衡逆向移动,所V正<V逆,故图象为: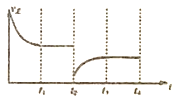 ,故答案为:
,故答案为: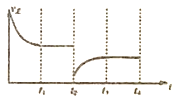 ;
;
(2)①1.2g 碳为0.1mol,则1molC反应吸收13.13kJ×10=131. 3kJ热量,该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3kJ·mol-1,故答案为:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.3kJ·mol-1;
②由于Ka2=5.61×10-11<Ka1=9.1×10-8<Ka1=4.30×10-7、Ka2=5.61×10-11>Ka2=1.1×10-12,所以氢硫酸能够与碳酸钠溶液反应生成碳酸氢钠和硫氢化钠,反应的离子方程式为:CO32-+H2S=HCO3-+HS-,故答案为:CO32-+H2S=HCO3-+HS-;
(3)①根据实验1计算平衡常数,
H2O(g)+CO(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
初始(mol/L) 1 2 0 0
转化(mol/L) 0.8 0.8 0.8 0.8
平衡(mol/L) 0.2 1.2 0.8 0.8
K=![]() =2.67,故答案为:2.67;
=2.67,故答案为:2.67;
②如果a=b两者的转化率相等,CO的转化率大于水蒸气,相当于加入水蒸气,平衡正向移动,则a<b,故答案为:a<b;
③根据实验2计算平衡常数,
H2O(g)+CO(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
初始(mol/L) 0.5 1 0 0
转化(mol/L)0.2 0.2 0.2 0.2
平衡(mol/L) 0.3 0.8 0.2 0.2
K=![]() =0.167,温度升高K变小,温度升高平衡向逆反应方向移动,正反应为放热反应,△H<0;按10mol CO,5mol H2O,2mol CO2,5mol H2,分别加入该容器,Qc=
=0.167,温度升高K变小,温度升高平衡向逆反应方向移动,正反应为放热反应,△H<0;按10mol CO,5mol H2O,2mol CO2,5mol H2,分别加入该容器,Qc=![]() =0.2>K,反应逆向进行,v(正)<v(逆),故答案为:>;<。
=0.2>K,反应逆向进行,v(正)<v(逆),故答案为:>;<。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】硅酸盐在地壳中分布很广,可用蛭石生产硫酸镁和氢氧化镁。某地蛭石的主要成分是[(Mg2.36Fe0.48Al0.16)(Si2.72Al1.28)O10(OH)2] ·[Mg0.32(H2O)0.42],还含有少量杂质FeO。
实验步骤如下:
Ⅰ.制取粗硫酸镁:用硫酸浸泡蛭石矿粉,过滤,将滤液结晶得到粗硫酸镁。
Ⅱ.提纯粗硫酸镁:将粗硫酸镁在酸性条件下溶解,加入适量的0.1mol·L—1H2O2溶液,再加试剂A调节溶液pH,并分离提纯。
Ⅲ.制取氢氧化镁:向步骤Ⅱ得的溶液中加入过量氨水。
一些金属离子转化为氢氧化物沉淀时溶液的pH如表1所示
表1
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
完全沉淀时 | 3.7 | 5.2 | 9.7 |
请回答:
(1)在步骤Ⅱ中加H2O2溶液的目的是___________。调节溶液pH的范围是______________。试剂A的最佳选择是_________(填字母序号)。
A、MgO B、Na2CO3 C、蒸馏水 D、稀硫酸
(2)测定粗硫酸镁中Fe2+的含量。称取12.3g粗硫酸镁样品溶于水形成溶液,完全转移到锥形瓶中,加稀硫酸酸化,滴加几滴黄色铁氰化钾K3[Fe(CN)6]溶液,用0.010 mol·L—1H2O2溶液进行滴定。平行测定4组,消耗H2O2溶液的体积数据记录如表2所示。
表2
实验编号 | 1 | 2 | 3 | 4 | 平均值 |
消耗H2O2溶液的体积/mL | 12.49 | 12.50 | 13.62 | 12.51 |
①K3[Fe(CN)6]与Fe2+反应生成带有特征蓝色的铁氰化亚铁沉淀,请写出反应的离子方程:________。
②反应达到终点时的标志是_________________________________________________。
③根据表2数据,可计算出粗硫酸镁样品中含有Fe2+_______________mol。
(3)工业上常以Mg2+的转化率为考查指标来确定步骤Ⅲ制备氢氧化镁工艺过程的适宜条件。
①步骤Ⅲ中制备氢氧化镁反应的离子方程式为_________________________。
②已知25℃时,Mg(OH)2和Ca(OH)2的Ksp分别为2×10-11和4.7×10—6。若用石灰乳替代氨水,__________(填“能”或“不能”)制氢氧化镁,理由是_____________________________。
③通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,Mg2+完全沉淀时溶液的pH为________。(保留小数点后一位)(已知lg2=0.3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法不正确的是
A. 9 g![]() 中含有的电子数为3.6 NA
中含有的电子数为3.6 NA
B. 某温度下纯水的pH=6,该温度下1L pH=11的NaOH溶液中含OH-的数目为0.1NA
C. 一定温度下,1 L 0.5 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1NH4Cl溶液含![]() 均为0.5NA
均为0.5NA
D. 丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 淀粉和纤维素都是纯净物
B. 油脂都不能使溴的四氯化碳溶液褪色
C. 蔗糖和淀粉都不能使新制氢氧化铜在加热条件下还原成红色沉淀
D. 羊毛、棉花的主要成分都是蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硬脂酸甘油酯经皂化反应得到硬脂酸钠和甘油。欲分离出硬脂酸钠应采取的正确方法及顺序是 ①过滤 ②分液 ③蒸馏 ④盐析 ⑤结晶 ( )
A. ④⑤ B. ④② C. ②③ D. ④①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图甲、乙、丙为组成生物体的相关化合物,乙为一个由α、β、γ三条多肽链形成的蛋白质分子,共含271个氨基酸,图中每条虚线表示由两个硫基(-SH)脱氢形成一个二硫键(-S-S-)。下列相关叙述不正确的是
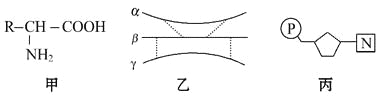
A. 甲为组成乙的基本单位,且乙中最多含有20种甲
B. 由不同的甲形成乙后,相对分子质量比原来少了4 832
C. 丙主要存在于细胞核中,且在乙的生物合成中具有重要作用
D. 如果甲中的R为C3H5O2,则由两分子甲形成的化合物中含有16个H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1∶2∶2∶3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是( )
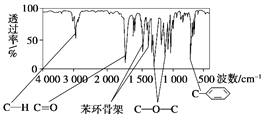
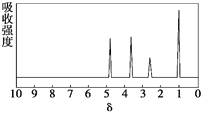
A. 符合题中A分子结构特征的有机物只有1种
B. A属于酯类化合物,在酸性条件下水解产物遇FeCl3溶液显紫色
C. A在一定条件下可与4 mol H2发生加成反应
D. 与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com