
���Ȼ��ף�PCl3����һ����Ҫ���л��ϳɴ�����ʵ���ҳ��ú���������Cl2��ȡPCl3��װ������ͼ��ʾ��
��֪������������Cl2��Ӧ����PCl3�������Cl2��Ӧ����PCl5��PCl3��O2������POCl3(��������)�� POCl3����PCl3��PCl3��ˮ��ǿ��ˮ������H3PO3��HCl��PCl3��POCl3���۷е���±���
| ���� | �۵�/�� | �е�/�� |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
| ʵ�鲽�� | ʵ������ | ʵ����� |
| �� | | ��ҺX�к���Na+ |
| �� | | ��ҺX�к���Cl- |
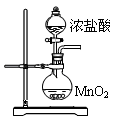
(1) Ũ���ᣨ1�֣����ն����Cl2����ֹ�����е�ˮ����������ƿ��PCl3��Ӧ����2�֣�
(2) �ž�װ���еĿ�������ֹ������ȼ����1�֣�
�ȹر�K1����K2����B����Һ�Ϸ���������ɫ�����K1���ر�K2����2�֣�
(3) ���� ��1�֣�
(4)
��5���Ѳ����ܿ���ˮ��ʪ��1�֣� û�У��þƾ��ƣ����� ��1�֣�ʵ�鲽�� ʵ������ ���ò�˿������������˿��պȡ��ҺX���ھƾ�������������(1��) ����ʻ�ɫ(1��) ��ȡ������ҺX����������ϡHNO3(1��)���ٵμ�����AgNO3��Һ(1��) ���ְ�ɫ������1�֣�
�������������
��1��BΪŨ���ᣬ��ʯ���������ն���������ͷ�ֹ������ˮ������װ�á�
��2��ͨCO2��Ŀ��Ϊ����װ�õĿ�����
��3������
��4���ο��ϱ���
��5��������װ��ʱ����Ҫ��ʪ��ʵ����������������ȡ�
���㣺������ʵ��Ļ���������ʵ����ƺͷ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�����12�֣�
�ҹ������������[(NH4)3PO4]�ŷŵķ�����ʯ��ȡ���Ტ����ˮ��ļ����о���óɹ�����֪��ʯ����Ҫ�ɷ���Ca3(PO4)2��������������������£�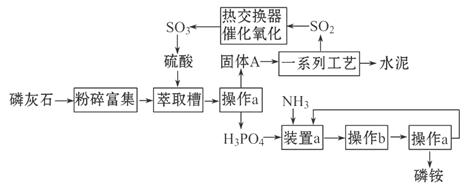
38������a��������___________��ʵ�����н��д˲����ķDz���������Ʒ��___________����ʵ�����в���b��������______________________��
39��װ��a������������ʽ�Σ����ǵĻ�ѧʽ�ֱ���_______________________��
40������A��һ�����е����ʣ��仯ѧʽ��_________________��
41���Ƚ�������ʵ�����Ƚ�����װ�á���ѧʵ����Ҳ���������Ƚ�����ʵ��ij��ʵ��Ŀ�ģ�����Һ�Ƚ���ʱͨ��ʹ�õ�������________________________��
42. ��������������β�����˺���N2��O2�⣬������SO2������SO3�������������ڲⶨ����β����SO2�������Լ���__________��
a��NaOH��Һ����̪��Һ b��KMnO4��Һ��ϡ����
c. ��ˮ��������Һ d����ˮ����̪��Һ
���õIJ�������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
���³�ѹ�£�O3Ϊ����ɫ�������ζ�����壬��ҵ�ϳ���O3��Ϊ��ֽ����֯����ҵ��Ư����ɫ����Ҳ����������ˮ��������ɱ��������O3Ũ�ȳ���ʱ������ǿ�����Զ�����������������á���Ȼ�����´���ʱ�����л��в���O2ת��ΪO3��
ʵ�������ṩ����װ�ú�ҩƷ���������O3���Ʊ���������֤ʵ�顣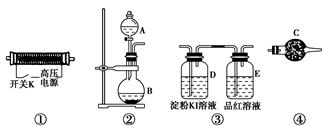
��ش��������⣺
(1)����װ�õ�����˳��Ϊ______��______��________��________��
(2)A��Ӧװ����Լ�Ϊ________(д��ѧʽ)��B�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________________________________��
(3)��������װ�õ������Եľ��������__________________________��
(4)ʵ�鿪ʼʱ��ȡ�·�Һ©�������ӣ��Ͽ���Դ����K����������Һ©���Ļ���������ͨ������һ��ʱ�䣬��Ŀ����________��________��Ȼ����ϵ�Դ����K����Ԥ������װ���п��ܹ۲쵽������Ӧ�Ľ��ۡ�
Dװ���У�___________________________________________________��
Eװ���У�____________________________________________________��
(5)��ָ����ʵ��װ���еIJ���֮�����Ľ���_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�����������ػ�ɫ�̼������壬�۵㣺��116�棬�е�3.8�森�������Ȳ��ȶ����Ӵ�һ���л����ױ�ը����������ˮ��1��100����ͬʱ��Ӧ���ɴ�������Һ���Ʊ���֮��Ҫ��ȴ�ɹ�̬�Ա���������森�Ʊ�����Cl2O�����ø����������HgO��Ӧ��������HgO?HgCl2����װ��ʾ����ͼ������̨�ͼг���������ȥ����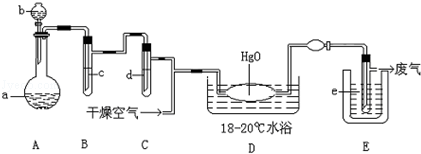
��1��A��ʢ�е���ɫ�����Լ�a���� ������Һ©�����Լ�b�� ����
��2��B��ʢ��Һ��c���� ����C�е�Һ��d���� ��
��3��D����������Ӧ�Ļ�ѧ����ʽ���� ��
��4��E�еı���ƿ��ʢ�����������Ӧ���� �����ڸɱ�����ˮ��Һ̬������ѡ����E���ڹܵõ������������п��ܺ����������� ��
��5��װ��A��B��C������ӷ�ʽ��D��E������ӷ�ʽ�����Ե��������������� ��������Щ��ͬ�����ӷ�ʽ����Ҫ�������� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
����̼��ƹ㷺Ӧ���������ϡ���ֽ����ѧ���ġ���ī��Ϳ�ϡ��ܷ⽺�뽺ճ������ҵ����ŨCaCl2��Һ��ͨ��NH3��CO2�������Ƶ�����̼��ơ�ijУѧ��ʵ��С�������ͼ��ʾװ�ã���ȡ�ò�Ʒ��D��װ��պϡ�������֬�ޣ�ͼ�мг�װ������ȥ��
��ѡ�õ�ҩƷ�У�
a��ʯ��ʯ��b�������Ȼ�����Һ��c��6 mol/L���d���Ȼ�泥�e����������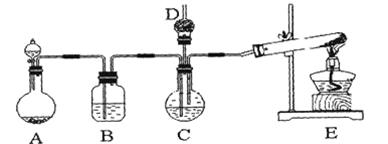
��1��A���Ʊ�����ʱ������ҩƷ�ǣ�ѡ����ĸ��ţ� ��
��2��B��ʢ�б���̼��������Һ���������� ��
��3��д����ȡ�����Ļ�ѧ����ʽ ��
��4����ʵ������У���C��ͨ�����������Ⱥ�˳��ģ�Ӧ��ͨ������Ļ�ѧʽ ��
��5������D���ڴ��Ƿ��а����ݳ��ķ����� ��
��6��д��������̼��ƵĻ�ѧ����ʽ ��
��7����ʵ��������а����ݳ���Ӧѡ������ װ�û��գ�����ţ���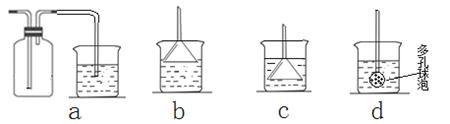
�������������Ȼ����Ʒ�к�������̼�����ơ�Ϊ�˲ⶨ�Ȼ�淋�������������ѧ��ʵ��С�������������ʵ�����̣�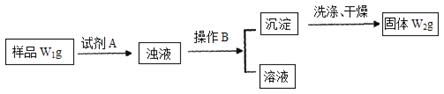
�Իش�
��1�������Լ�A�Ļ�ѧʽΪ
��2��B����������
��3����Ʒ���Ȼ�淋���������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�ߴ��ȵ������ǵ��͵����ǽ������ϣ����Ʊ��뵼�����Ҫ���ϣ����ķ��ֺ�ʹ��������������һ�������������ߴ���ͨ�������·����Ʊ�����̼�ڸ����»�ԭ���������Ƶôֹ裨��Fe��Al��B��P�����ʣ����ֹ���������Ӧ�������Ȼ��裨��Ӧ�¶�Ϊ450��500�棩�����Ȼ��辭�ᴿ����������ԭ�ɵøߴ��衣������ʵ�����Ʊ����Ȼ����װ��ͼ��
�����Ϣ��a�����Ȼ�����ˮ����ˮ�⣻b���������������ڸ����¾���������ֱ�ӻ���������Ӧ���Ȼ��c���й����ʵ������������±���
| ���� | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| �е�/�� | 57.7 | 12.8 | �� | 315 | �� |
| �۵�/�� | ��70.0 | ��107.2 | �� | �� | �� |
| �����¶�/�� | �� | �� | 180 | 300 | 162 |
| ���� | ����֮�� |
| �� | |
| �� | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
������ͭ�Ǵ���ˮ�潢������Ϳ�����Ҫԭ�ϡ�ijС����������о�������д���пհס�
ʵ��1��������ͭ����ȡ������ͭ���������Ǻ�����������ͭ����Һ��Ӧ��ȡ�����ױ������������Ʋ���ʱ��������CuO���ɡ�
��1��ʵ������ȡ������ͭ����Һ�����ӷ���ʽΪ____________��
��2��ʵ�����ô˷�����ȡ���������������ͭ���壬��Ҫ�IJ����������Թܡ��ƾ��ơ��ձ�____________��____________��
��3����Ҫ̽���÷�Ӧ����������¶ȣ�Ӧѡ�õļ��ȷ�ʽΪ____________��
ʵ��2���ⶨ������ͭ�Ĵ���
����1����ȡʵ��1���ù���m g����������װ�ý���ʵ�顣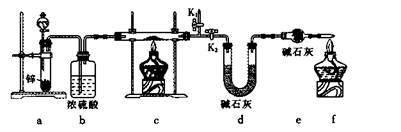
��4��װ��a�����ӵ�����____________���ѧʽ����
��5��ͨ������������������ܴﵽʵ��Ŀ�ĵ���____________��
| A����Ӧǰ��װ��a������ |
| B��װ��c��ַ�Ӧ�����ù�������� |
| C����Ӧǰ��װ��d������ |
| D����Ӧǰ��װ��e������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��������AIN����һ�����������ϣ��㷺Ӧ���ڼ��ɵ�·��������ij��ѧ�о�С�����õ������������ͻ���̿��ȡ�������������ͼʵ��װ�á�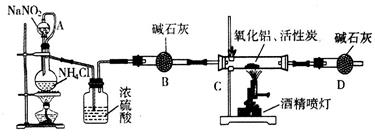
�Իش�
��1��ʵ�����ñ���NaNO2�� NH4C��Һ��ȡ�����Ļ�ѧ����ʽΪ ��
��2��װ���з�Һ©����������ƿ֮��ĵ���A�������� ����д��ţ���
a.��ֹNaNO2������Һ���� b.��֤ʵ��װ�ò�©�� c.ʹNaNO2������Һ������
��3����ͼ���Ӻ�ʵ��װ�ã����װ�������Եķ����� ��
��4����ѧ�о�С���װ�ô����������⣬��˵���Ľ��İ취 ��
��5����Ӧ������ijͬѧ����ͼװ�ý���ʵ�����ⶨ��������Ʒ������������ʵ���е���������Բ��ƣ�����֪����������NaOH��Һ��Ӧ����Na[Al(OH)4]�Ͱ���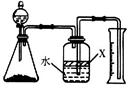 ��
��
�ٹ��ƿ�е��Լ�X���ѡ�� ����д��ţ���
a.���� b.�ƾ� c.ֲ���� d.CCl4
�ڹ��ƿ�е�Һ��û��װ�����Ϸ����пռ䣩����ʵ����NH3������� ���ƫ����ƫС���������䡱����
����ʵ���г�ȡ��������Ʒ������Ϊ10.0g����ð��������Ϊ3.36L����״����������Ʒ��AlN����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����й�ʵ�����������ͽ��ͻ���۶���ȷ����(����)
| ѡ�� | ʵ����� | �֡��� | ���ͻ���� |
| A | ������Fe���м���ϡHNO3����ַ�Ӧ����KSCN��Һ | ��Һ�ʺ�ɫ | ϡHNO3��Fe����ΪFe3�� |
| B | AgI�����е���ϡKCl��Һ | �а�ɫ�������� | AgCl��AgI������ |
| C | Al������ϡHNO3�� | ������ | Al�����汻HNO3�������γ����ܵ�����Ĥ |
| D | �ò�����պȡŨ��ˮ�㵽��ɫʯ����ֽ�� | ��ֽ����ɫ | Ũ��ˮ�ʼ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com