
【题目】白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成下列实验的是:
①检验自来水中是否含氯离子 ②鉴别食盐和小苏打
③蛋壳是否含碳酸钙 ④白酒中是否含甲醇 ( )
A. ①② B. ①④ C. ②③ D. ③④
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁:另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的物质的量浓度为( )
A.(4b﹣2a)/V molL﹣1
B.(b﹣2a)/V molL﹣1
C.(2b﹣2a)/V molL﹣1
D.(b﹣a)/V molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4mo1A和2molB进行如下反应:
3A(g)+2B(g)![]() 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后的压强之比为5:4 (相同的温度下测量), 则下列说法正确的是
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后的压强之比为5:4 (相同的温度下测量), 则下列说法正确的是
A. 该反应的化学平衡常数表达式是![]()
B. 此时,B 的平衡转化率是35%
C. 增大该体系的压强,平衡向右移动化学平衡常数增大
D. 增加C的量,B的平衡转化率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA.下列说法正确的是( )
A. 1L0.1molL﹣1NH4Cl溶液中,NH4+的数量为0.1NA
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1NA
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(l)在下列事实中,什么因素影响了化学反应的速率?
①熔融的KClO3放出气泡很慢,撒入少量MnO2很快产生气体______;
②同浓度、同体积的盐酸中放入同样大小的锌粒和镁粒,产生气体有快有慢______;
③KI晶体和HgCl2晶体混合后无明显现象,若一起投入水中,很快生成红色HgI2______;
(2)某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。限选试剂:1.00 mol/LHNO3、2.00 mol/LHNO3,细颗粒大理石、粗颗粒大理石,35℃水浴。
①请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
实验编号 | T℃ | 大理石规格 | HNO3浓度(mol/L) |
A | 常温 | 2.00 | |
B | 粗颗粒 | 1.00 | |
C | 粗颗粒 | 2.00 | |
D | 细颗粒 | 2.00 |
②整个实验中应控制的不变量是硝酸溶液体积和______。
③该实验小组用如右图实验装置进行实验。

a.除电子天平、干燥管、锥形瓶、药匙、胶塞等仪器外,必需的实验仪器还有______。
b.若反应开始时电子天平读数为100.00g,经2分钟反应结束时的读数为95.60g,则这两分钟内用CaCO3来表示的速率为_____g/min。
c.若撤除干燥管装置,所测速率______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,在2 L的密闭容器中,气体X、Y和Z三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是
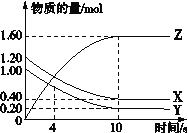
A.容器中化学反应为X(g)+Y(g)![]() Z(g)
Z(g)
B.0~10 s,X表示的平均化学反应速率为0.04 mol/(L·s)
C.使用催化剂只能加快0~10 s间的反应速率
D.0~4 s的平均反应速率小于0~10 s的平均反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的有( )个
①反应速率用于衡量化学反应进行的快慢
②可逆反应达到化学平衡状态时,正、逆反应速率都为0
③决定反应速率的主要因素是反应物的性质
④适当增大反应物浓度,提高反应温度都能增大反应速率
⑤不管什么反应使用催化剂,都可以加快反应速率 ,并可以使平衡移动。
⑥可逆反应A(g)![]() B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强,正反应速率减小,逆反应速率增大
⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大
A. 2 个 B. 3 个 C. 4 个 D. 5个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com