

图3-8
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:2014届江苏省启东市高二上学期期末考试化学试卷(解析版) 题型:填空题
(1)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)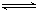 CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。某科学实验将6molCO2和8molH2充入2L密闭容器中,测得H2的物质的量随时间变化如右图所示(实线)。图中数据a(1,6)代表的意思是:在l min时H2的物质的量是6mol。
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。某科学实验将6molCO2和8molH2充入2L密闭容器中,测得H2的物质的量随时间变化如右图所示(实线)。图中数据a(1,6)代表的意思是:在l min时H2的物质的量是6mol。
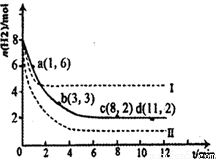
①下列时间段平均反应速率最大的是__________,最小的是______________。
A.0~1min B.1~3min C.3~8min D.8~11min
②仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示,曲线Ⅰ对应的实验改变的条件是________,曲线Ⅱ对应的实验改变的条件是_________。
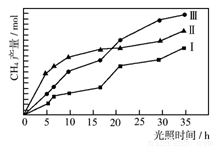
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,等量的CO2和H2O(g)在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图所示。在0~30 h内,CH4的平均生成速率v(Ⅰ)、v(Ⅱ)和v(Ⅲ)从大到小的顺序为 。反应开始后的12小时内,在第___________种催化剂的作用下,收集的CH4最多。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省沈阳市高三模拟考试理科综合化学试卷(解析版) 题型:填空题
(17分)I.工业上有一种用CO2来生产甲醇燃料的方法:
将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。图中数据a(1,6)表示:在1 min时H2的物质的量是6 mol。

(1)a点正反应速率 (填“大于”“等于”或“小于”)逆反应速率。其化学平衡常数K=
(2)下列时间段平均反应速率最大的是 ,
A.O~1 min B.1~3 min C.3~8 min D.8~11 min
(3)仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示。曲线I对应的实验条件改变是 ,曲线Ⅱ对应的实验条件改变是 ,体积不变再充入3molCO2和4 mol H2,H2O(g)的体积分数 (填“增大”“不变”或“减小”)
Ⅱ.某实验小组欲探究 反应速率与温度的关系,现有1mol/L的KI溶液、0.1mol/L的H2S04溶液、淀粉溶液,则实验时这几种试剂的加入顺序为:KI溶液、 、 ;
反应的方程式为
Ⅲ. 粗镍样品中含Fe、Zn、Ag、Cu等四种金属杂质,为获得高纯度的镍,某兴趣小组同学拟用铅蓄电池为电源,粗镍及石墨为电极,电解硝酸镍溶液对粗镍进行提纯。
(1)电解结束后,在阳极附近的沉淀物中,主要的金属单质为 (填化学式)。

(2) 若按上图所示连接对铅蓄电池进行充电。充电一段时间后。则在A电极上生成 (填化学式)。B电极上的电极反应式为 ;充电完毕。铅蓄电池的正极是 极(填“A”或“B”)。
(3)如用甲烷燃料电池为电源,在25℃、101 kPa时,若CH4在氧气中直接燃烧生成1 mol水蒸气放热401 kJ,而l g水蒸气转化成液态水放热2.445 kJ,则CH4的燃烧热为 (取整数)kJ·mol-。
查看答案和解析>>
科目:高中化学 来源: 题型:
现代工业将煤炭气化后,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以制成许多清洁能源、扩大水煤气的广泛用途。
(1)已知:①2C(s)+O2(g)=2CO(g) △H1=-221.0kJ.mol-1;
②2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ.mol-1
则反应C(s)+ H2O(g)= CO(g) + H2(g);△H=____ 。
(2)工业上有一种用CO2 来生产甲醇燃料的方法: CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1
 现将6.0molCO2和8.0molH2充入2L的密闭容器中,测得H2的物质的量(n)随时间变化如下图所示(实线)。
现将6.0molCO2和8.0molH2充入2L的密闭容器中,测得H2的物质的量(n)随时间变化如下图所示(实线)。
①下列时间段平均反应速率最大的是______(填序号),
A.0~1min B.1~3min
C.3~8min D.8~11min
其速率是:υ(H2)=_________ 。
② 平衡时氢气的转化率 ;该条件下
反应的平衡常数K= 。
③仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是___________,曲线II对应的实验条件改变是_____________。
(3)某研究所组装的CH3OH—O2燃料电池的
工作原理如图所示。

①该电池工作时,b口通入的物质为 ,
②该电池正极的电极反应式为: 。
 ③以此电池做电源,在实验室中模拟铝制品表面
③以此电池做电源,在实验室中模拟铝制品表面
“钝化”处理(装置右图所示)的过程中,发现溶液
逐渐变浑浊并有气泡产生,其原因可能是
(用相关的离子方程式表示):
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com