
| 12 |
| 13 |
| 70.59% |
| 12 |
| 5.88% |
| 1 |
| 23.53% |
| 16 |
| 12 |
| 13 |
| 70.59% |
| 12 |
| 5.88% |
| 1 |
| 23.53% |
| 16 |
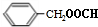 或
或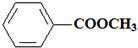 ,B能与碳酸氢钠反应,含有羧基,而C不能,C为醇,则B为甲酸或苯甲酸,结构简式为HCOOH或
,B能与碳酸氢钠反应,含有羧基,而C不能,C为醇,则B为甲酸或苯甲酸,结构简式为HCOOH或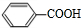 ,对应的C为苯甲醇或甲醇,结构简式为
,对应的C为苯甲醇或甲醇,结构简式为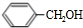 或CH3OH,
或CH3OH,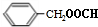 或
或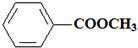 ,B的结构简式为HCOOH或
,B的结构简式为HCOOH或 ,对应C得到结构简式为
,对应C得到结构简式为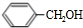 或CH3OH.
或CH3OH.


科目:高中化学 来源: 题型:
| A、Al3+,Na+,NO3-,Cl- |
| B、K+,Na+,Cl-,NO3- |
| C、K+,Na+,Cl-,CH3COO- |
| D、K+,NH4+,SO42-,NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
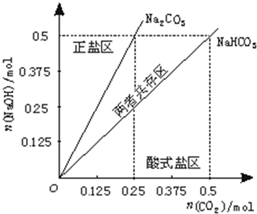 用NaOH、H2O、大理石和盐酸制取33g纯NaHCO3,请参照物质的溶解度回答下列问题:
用NaOH、H2O、大理石和盐酸制取33g纯NaHCO3,请参照物质的溶解度回答下列问题:| 25℃ | 溶解度/g |
| NaOH | 100 |
| NaHCO3 | 9 |
| Na2CO3 | 30 |
| n(CO2) |
| n(NaOH) |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
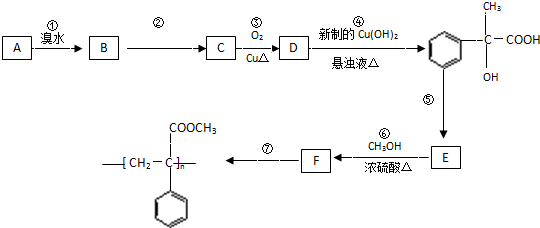
查看答案和解析>>
科目:高中化学 来源: 题型:
| y-x |
| 2 |
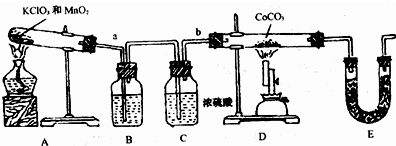
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A=B |
| B、A=10-4 B |
| C、B=10-4 A |
| D、无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com