
| A. | 加入NaOH溶液产生红褐色沉淀,则原溶液中一定有FeCl3 | |
| B. | 加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中一定是CO32-或SO32- | |
| C. | 先通入少量Cl2后,再加入淀粉溶液后,溶液变蓝,说明有I- | |
| D. | 往溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成,说明一定有SO42- |
分析 A.无色溶液中一定不存在铁离子;
B.能使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫;
C.氯气能置换碘单质,碘遇淀粉溶液变蓝色;
D.能使氯化钡产生白色沉淀的离子有碳酸根离子、硫酸根离子和亚硫酸根离子,但碳酸钡能溶于稀硝酸,亚硫酸钡能被氧化为硫酸钡.
解答 解:A.和碳酸钠反应生成能白色沉淀的阳离子不一定是钙离子,也可能是钡离子,故A错误.
B.能使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫,能和盐酸反应生成能使澄清石灰水变浑浊的气体的阴离子有碳酸根离子、碳酸氢根离子、亚硫酸根离子、亚硫酸氢根离子,故B错误;
C.氯气能置换碘单质,碘遇淀粉溶液变蓝色,所以通入少量Cl2后,溶液变为黄色,再加入淀粉溶液后,溶液变蓝,说明有I-,故C正确;
D.稀硝酸有强氧化性,能把亚硫酸盐氧化成硫酸盐,所以往溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成,原溶液中可能含有SO32-,不一定含有SO42-,故D错误;
故选C.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质及检验方法为解答关键,D为易错点,注意稀硝酸有强氧化性,能把亚硫酸盐氧化成硫酸盐,试题培养了学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O和Na2O2 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

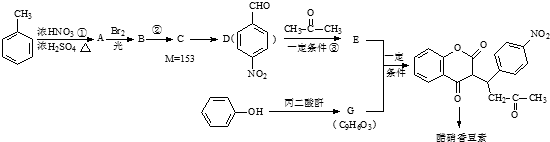

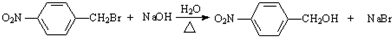 ;
;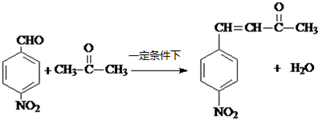 ;
;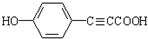 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al最外层电子数依次增多,其还原性依次增强 | |
| B. | P、S、Cl最高正价依次升高,对应气态氢化物稳定性依次增强 | |
| C. | C、N、O原子半径依次增大 | |
| D. | Na和K属于第ⅠA族元素,其氧化物的水化物碱性:NaOH比KOH强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
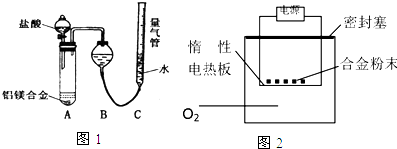
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
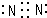 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
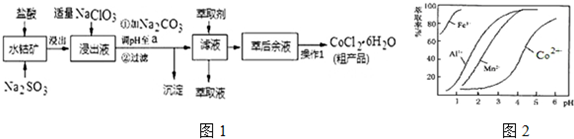
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com