
 用隔膜电解法处理高浓度乙醛废水的原理是使乙醛分别在两极发生反应,转化为乙醇和乙酸.实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.有关说法不正确的是( )
用隔膜电解法处理高浓度乙醛废水的原理是使乙醛分别在两极发生反应,转化为乙醇和乙酸.实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示.有关说法不正确的是( )| A、图中燃料电池的a极应通入氧气 |
| B、乙醇在阴极产生 |
| C、电解过程中,阴极区有NaOH产生 |
| D、每生成1mol乙酸,理论上至少消耗标况下氧气22.4L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、银质物品久置表面变暗 |
| B、远洋海轮的尾部装上一定数量的锌板 |
| C、常温条件下,在空气中铝不易被腐蚀 |
| D、用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol Na2O2固体中含有离子总数为3 NA |
| B、常温常压下,3.2gCH4中含有电子2 NA |
| C、标准状况下,28g N2和CO所组成的混合气体,其体积为22.4L |
| D、足量铁粉与1molCl2在加热条件下充分反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 和
和 为原料制备
为原料制备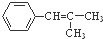 的合成路线流程图(无机试剂任用).合成路线流程图示例如图:
的合成路线流程图(无机试剂任用).合成路线流程图示例如图:| NaOH溶液 |
| △ |
| CH3COOH |
| 浓硫酸△ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知25℃时有关弱酸的电离平衡常数:
已知25℃时有关弱酸的电离平衡常数:| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com