
一定温度下,在一定容积的密闭容器中发生如下可逆反应:
2A(g)+B(g) 2C(g) ,在反应过程中,C的物质的量n(C)随时间的变化关系如下图所示(从t1时间开始对反应体系升高温度)。试回答下列问题:
2C(g) ,在反应过程中,C的物质的量n(C)随时间的变化关系如下图所示(从t1时间开始对反应体系升高温度)。试回答下列问题:
(1)a点时,反应的v(正) v(逆)(填“>”、“<”或“=”);
(2)此反应的逆反应为 热反应(填“放”或“吸”);
(3)a、b两点的正反应速率:v(a) v(b)
(填“>”、“<” 或“=”)。
科目:高中化学 来源: 题型:
等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入等质量的铝,生成氢气的体积比为5∶6,则甲、乙两烧杯中的反应情况可能分别是( )。
A.甲、乙中都是铝过量 B.甲中铝过量:乙中碱过量
C.甲中酸过量、乙中铝过量 D.甲中酸过量、乙中碱过量
查看答案和解析>>
科目:高中化学 来源: 题型:
V1ml、0.2 mol/L Na2SO4溶液和V2ml、0.1 mol/L Fe2(SO4)3溶液混合,已知V1
大于V2 ,则混合溶液中SO42-的物质的量浓度可能是
A. 0.23 mol/L B.0.18 mol/L C.0.26 mol/L D.0.25 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.单质铯的熔点比单质锂的高 B.胶体的胶粒不能通过滤纸
C.元素N的氢化物的沸点比元素P的氢化物的沸点低
D.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
查看答案和解析>>
科目:高中化学 来源: 题型:
蓄电池在放电时起原电池作用,在充电时起电解池的作用。下式是爱迪生蓄电池分别在充电和放电时的反应:
则下列有关对爱迪生蓄电池的推断错误的是
A.放电时正极附近pH增大
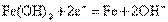 B.充电时阴极的电极反应式为:
B.充电时阴极的电极反应式为:
C.放电时电解质溶液中的阴离子向正极方向移动
D.蓄电池的电极可浸入某种碱性电解质溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色溶液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则原溶液中
A.一定溶有CO32- B.一定溶有Ag+
C.一定溶有SO42- D.可能溶有SO42-,也可能溶有Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列有关实验得出的结论一定正确的是
| 选项 | 操作 | 现象与结论 |
| A | 同温时,等质量的锌粒分别与足量稀硫酸反应 | 产生H2,氢气量:加胆矾=未加胆矾 |
| B | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液 | 溶液变黄,氧化性:H2O2>Fe3+ |
| C | 相同温度下,等质量的大理石与等体积、等浓 度的盐酸反应 | 粉状大理石产生气泡更快, 反应速率:粉状大理石>块状大理石 |
| D | 向浓度均为0.1 mol·L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀, Ksp(AgCl)<Ksp(AgI) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com