
下列物质中属于强电解质且能导电的是
①氢氧化钠溶液 ②硫酸钙固体 ③铜 ④蔗糖 ⑤三氧化硫 ⑥熔融氯化钠
A.①②⑤ B.①②⑥ C.③⑥ D.⑥
科目:高中化学 来源: 题型:
下图是一个化学过程的示意图。
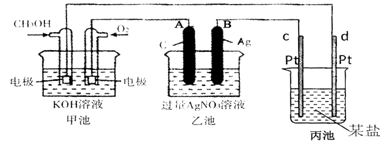
(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH的电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出0.64g某金属,则丙中的某盐溶液可能是 (填序号)
A. MgSO4 B.CuSO4 C.NaCL D.AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在一定容积的密闭容器中发生如下可逆反应:
2A(g)+B(g) 2C(g) ,在反应过程中,C的物质的量n(C)随时间的变化关系如下图所示(从t1时间开始对反应体系升高温度)。试回答下列问题:
2C(g) ,在反应过程中,C的物质的量n(C)随时间的变化关系如下图所示(从t1时间开始对反应体系升高温度)。试回答下列问题:
(1)a点时,反应的v(正) v(逆)(填“>”、“<”或“=”);
(2)此反应的逆反应为 热反应(填“放”或“吸”);
(3)a、b两点的正反应速率:v(a) v(b)
(填“>”、“<” 或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
①铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+
②Cu(OH)2和HNO3混合:H++OH-===H2O
③Fe与稀硝酸反应 Fe+2H+==Fe2++H2↑
④H2SO3与氢氧化钠混合 H++OH-==H2O
⑤碳酸钡与稀盐酸反应: BaCO3+2H+==Ba2++H2O+CO2↑
⑥SO3溶于水:SO3+H2O==2H++SO42-
A.③⑤⑥ B.⑤⑥ C.①③④ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列三个反应的化学方程式,判断有关物质的还原性的强弱顺序
①I2 + SO2 + 2H2O == H2SO4 + 2HI
②2FeCl2 + Cl2 == 2FeCl3
③2FeCl3 + 2HI == 2FeCl2 + I2 + 2HCl
A. I- > Fe2+ >Cl- >SO2 B. Cl- > Fe2+ > SO2 >I-
C. Fe2+ >I- >Cl- >SO2 D. SO2 >I- > Fe2+ >Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组对加碘食盐中的KIO3进行研究,它是一种白色粉末,常温下很稳定,加热至560 ℃开始分解。在酸性条件下KIO3是一种较强的氧化剂,与HI、H2O2等作用,被还原为碘单质。
(1)学生甲设计实验测出加碘食盐中碘元素的含量,步骤如下:
a.称取w g加碘盐,加适量蒸馏水溶解; b.用稀硫酸酸化,再加入过量KI溶液;
c.以淀粉为指示剂,用物质的量浓度为1.00×10-3 mol·L-1的 Na2S2O3溶液滴定(滴定时的反应方程式:
I2+2S2O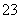 ===2I-+S4O
===2I-+S4O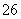 )。
)。
操作b涉及的主要反应的离子方程式为 ▲ ;滴定时,Na2S2O3溶液应放在 ▲ (填“酸式滴定管”或“碱式滴定管”),滴定至终点时消耗Na2S2O3溶液20.00 mL,其终点颜色变化为 ▲ ;加碘食盐样品中的碘元素含量是 ▲ mg·kg-1(以含w的代数式表示)。
(2)学生乙对纯净的NaCl(不含KIO3)进行了下列实验:
| 顺序 | 步骤 | 实验现象 |
| ① | 取少量纯净的NaCl,加蒸馏水溶解 | 溶液无变化 |
| ② | 滴入淀粉KI溶液,振荡 | 溶液无变化 |
| ③ | 放置片刻,再滴加稀H2SO4,振荡 | 溶液变蓝色 |
请推测实验③中产生蓝色现象的可能原因是(用离子方程式表示): ▲ 。由学生乙的实验结果推知,学生甲的实验结果将 ▲ (填“偏大、偏小或无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com