
ij��ѧ��ȤС��Լӵ�ʳ���е�KIO3�����о�������һ�ְ�ɫ��ĩ�������º��ȶ���������560 �濪ʼ�ֽ⡣������������KIO3��һ�ֽ�ǿ������������HI��H2O2�����ã�����ԭΪ�ⵥ�ʡ�
(1)ѧ�������ʵ�����ӵ�ʳ���е�Ԫ�صĺ������������£�
a����ȡw g�ӵ��Σ�����������ˮ�ܽ⣻ b����ϡ�����ữ���ټ������KI��Һ��
c���Ե���Ϊָʾ���������ʵ���Ũ��Ϊ1.00��10��3 mol��L��1�� Na2S2O3��Һ�ζ�(�ζ�ʱ�ķ�Ӧ����ʽ��
I2��2S2O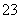 ===2I����S4O
===2I����S4O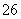 )��
)��
����b�漰����Ҫ��Ӧ�����ӷ���ʽΪ �� ���ζ�ʱ��Na2S2O3��ҺӦ���� �� (���ʽ�ζ��ܡ���ʽ�ζ��ܡ�)���ζ����յ�ʱ����Na2S2O3��Һ20.00 mL�����յ���ɫ�仯Ϊ �� ���ӵ�ʳ����Ʒ�еĵ�Ԫ�غ����� �� mg��kg��1(�Ժ�w�Ĵ���ʽ��ʾ)��
(2)ѧ���ҶԴ�����NaCl������KIO3������������ʵ�飺
| ˳�� | ���� | ʵ������ |
| �� | ȡ����������NaCl��������ˮ�ܽ� | ��Һ�ޱ仯 |
| �� | �������KI��Һ���� | ��Һ�ޱ仯 |
| �� | ����Ƭ�̣��ٵμ�ϡH2SO4���� | ��Һ����ɫ |
���Ʋ�ʵ����в�����ɫ����Ŀ���ԭ���ǣ������ӷ���ʽ��ʾ���� �� ����ѧ���ҵ�ʵ������֪��ѧ����ʵ������ �� ���ƫ��ƫС����Ӱ�족����
��֪ʶ�㡿�ȡ��塢�⼰�仯������ۺ�Ӧ�ã��������ʵĺ���
���𰸽�������1��5I-+IO3-+6H+ =3I2+3H2O ��ʽ�ζ��ܡ���ɫ����ɫ���ұ��ְ���Ӳ���ɫ��1270/3W
��2��4I����O2��4H+ �� 2H2O +I2�� ƫ��
����������1����ϡ�����ữ���ټ������KI��Һ��b�漰����Ҫ��Ӧ�����ӷ���ʽΪ5I-+IO3-+6H+ =3I2+3H2O��Na2S2O3Ϊǿ�������Σ���Ϊ������������ˮ�⣬Na2S2O3��Һ�������ԣ����Եζ�ʱNa2S2O3��ҺӦ���ڼ�ʽ�ζ����У�
b��������I2��c����ʹ�õ�����Ϊָʾ����������ۣ���Һ����ɫ����Na2S2O3��Һ�ζ���I2��Ӧ��ϣ���Һ��ɫ��ɫ���ζ��յ�����Ϊ����Һ��ɫ��ɫ��������ڲ��ָ���ɫ��
20mL��Һ����Na2S2O3�����ʵ���Ϊ1.00��10-3mol/L��0.02L=2.00��10-5mol������IO3-+5I-+6H+=3I2+3H2O��I2+2S2O32-=2I-+S4O62-����
IO3-��3I2��6S2O32-
1 6
xmol 2.00��10-5mol
���X=2.00��10-5��6���ӵ�ʳ����Ʒ�еĵ�Ԫ�غ�����2.00��10-5��6��127��106��W=1270/3W��mg��kg��1��
��2�����������£������ӱ������������ɵⵥ�ʣ����ӷ�Ӧ����ʽΪ��4I-+4H++O2=2I2+2H2O�������������£������ĵ������ױ������������������ɵⵥ�ʣ���b����ϡ�����ữ���ټ������KI��Һ�����Ե��²ⶨ���ƫ��
��˼·�㲦�������Ե�����е�IJⶨΪ���忼����������ԭ�ζ���Ӧ�á���ʵ��ԭ�����⣬ע�����յ⼰�仯����������ǽ����Ĺؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������������ǿ��������ܵ������
������������Һ ������ƹ��� ��ͭ ������ ���������� �������Ȼ���
A���٢ڢ� B���٢ڢ� C���ۢ� D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���Ƶ�˼ά�����ڻ�ѧѧϰ���о�����ʱ���������Ľ��ۣ�������ƵĽ�������Ҫ����ʵ���ļ������ȷ������ȷ������м������ƽ����У�������ǣ� ��
������ˮ��Ӧ����NaOH��H2�����н�����ˮ��Ӧ�����ɼ��H2��
����¶���ڿ�����һ��ʱ���ͻ����⣻���ʸ����õ��������ȶ������ڿ����С�
�ۻ�����NaCl�Ļ�����ɫΪ��ɫ��Na2CO3�Ļ�����ɫҲΪ��ɫ��
���ܶ�Ϊ1.1 g��cm��3���ܶ�Ϊ1.2 g��cm��3��NaCl��Һ�������ϣ�����NaCl��Һ���ܶȽ���1.1 g��cm ��3��1.2 g��cm��3֮�䣻Na��K�Ͻ���۵�Ӧ����Na��K���۵�֮�䡣
A���٢� B���٢� C���٢ڢۢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������һ����ɫ��������������Դ��ͼ������ɫ��Դ��ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��a��b��Ϊ��
����Pt�缫�����õ�ع���ʱ������˵���������
A��a�缫Ϊ�õ�ظ���
B��O2��b�缫�ϵõ��ӣ�������
C����ع���ʱ��a�缫��Ӧʽ��
CH3OCH3��12e��+3H2O��2CO2��+12H+
D����ع���ʱ��ȼ�ϵ���ڲ�H+��a�缫����b�缫
 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������й�ʵ��ó��Ľ���һ����ȷ����
| ѡ�� | ���� | ��������� |
| A | ͬ��ʱ����������п���ֱ�������ϡ���ᷴӦ | ����H2�����������ӵ�����δ�ӵ��� |
| B | ��Fe(NO3)2��Һ�е��������ữ��H2O2��Һ | ��Һ��ƣ������ԣ�H2O2��Fe3�� |
| C | ��ͬ�¶��£��������Ĵ���ʯ����������Ũ �ȵ����ᷴӦ | ��״����ʯ�������ݸ��죬 ��Ӧ���ʣ���״����ʯ����״����ʯ |
| D | ��Ũ�Ⱦ�Ϊ0.1 mol��L��1NaCl��NaI�����Һ�еμ�����AgNO3��Һ | ���ֻ�ɫ������ Ksp(AgCl)��Ksp(AgI) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ձ��м�ˮ�ͱ����ܶȣ�0.88 g��cm3����50 mL����һС�������ƣ��ܶȣ�0.97 g��cm3��Ͷ���ձ��У��۲쵽����������ǣ� ��
A������ˮ���з�Ӧ���Ĵ��ζ�
B����ͣ���ڱ����в�������Ӧ
C�����ڱ���Һ���Ϸ�Ӧ���Ĵ��ζ�
D�����ڱ���ˮ�Ľ��洦��Ӧ�������ϡ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾ����MgCl2��AlCl3�Ļ����Һ�м���NaOH��Һ������ʱ���������ʵ���y mol�����NaOH��Һ����������x mL�Ĺ�ϵͼ������ͼʾ�жϣ����н����в���ȷ���ǣ� ��
A��N��ʱ��Һ�е�����ֻ��NaCl
B��ԭ�����Һ��c (MgCl2)��c (AlCl3)=1��2
C��c (NaOH)=c (HCl)
D��M��֮ǰ�������NaOH��Һ��M��֮������������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��2CO(g)+O2(g)=2CO2 (g) ��H= -566 kJ��mol-1
Na2O2(s)+CO2(g)=Na2CO3 (s)+ 1/2O2 (g) ��H= -226 kJ��mol-1
���������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ����
A��CO��ȼ����Ϊ283 kJ
B����ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ
C��2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ��H= - 452 kJ/mol
D��CO(g)��Na2O2(s)��Ӧ�ų�509 kJ����ʱ������ת����Ϊ2x6.02��l023

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����
A��һ���¶ȡ�ѹǿ�£��������������ӵĴ�С����
B��һ���¶ȡ�ѹǿ�£���������������ʵ����Ķ��پ���
C������Ħ�������ָ1 mol�κ�������ռ�����Ϊ22.4 L
D����ͬ�����壬��������ȣ������������ķ�����һ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com