
【题目】锂常用来制造高能量电池。已知锂的金属性介于钠和镁之间,则冶炼金属锂应采用的方法
A. 热还原法 B. 热分解法 C. 电解法 D. 铝热法
科目:高中化学 来源: 题型:
【题目】钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为:2Na+xS=Na2Sx,电池结构如图所示。下列说法不正确的是( )

A. 放电时,Na作负极,反应式为Na-e-=Na+ B. 钠硫电池在常温下也能正常工作
C. 放电时Na+向正极移动 D. 当外电路通过0.25mol电子时消耗16g硫,则x=4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验中若使某步中的有害产物作为另一步的反应物,形成一个循环,则可不再向环境排放该种有害物质。在如图所示有编号的反应中,属于氧化还原反应的有

A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列叙述正确的是( )
A. 血红蛋白、牛胰岛素、蚕丝、人造奶油充分水解均可得到氨基酸
B. “光化学烟雾”、“臭氧空洞”、“温室效应"、“酸雨”的形成都与氮氧化合物有关
C. 天然气、沼气、酒精、水煤气均属于可再生能源
D. 用脱硫处理的煤代替原煤作燃料不能有效减少空气中CO2含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有1 mol KAl(SO4)2的溶液中逐滴加入氢氧化钡溶液,充分反应。下列说法不正确的是
A.当Al3+恰好完全沉淀时,消耗氢氧化钡1.5 mol
B.当![]() 恰好完全沉淀时,铝元素全部以偏铝酸根离子的形式存在
恰好完全沉淀时,铝元素全部以偏铝酸根离子的形式存在
C.当向溶液中加入1.5 mol氢氧化钡时,反应可用下列离子方程式表示:2Al3++3![]() +3Ba2++6OH
+3Ba2++6OH
===2Al(OH)3↓+3BaSO4↓
D.随加入的氢氧化钡的物质的量不断增大,沉淀的物质的量不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由 Al、Cu、Fe 三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________方法区分晶体、准晶体和非晶体。
(2)基态Fe原子有________个未成对电子。Fe3+的电子排布式为_______________。
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为________,1 mol乙醛分子中含有的σ键的数目为________。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有__________个铜原子。锗也是一种半导体材料,Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键,从原子结构角度分析,原因是______________________________。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图:

镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=________(填数值);氢在合金中的密度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,铁是使用最广泛的金属之一,已知在高温下,Fe与水蒸气可发生反应。
应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。

请回答下列的问题。
(1)铁在周期表中的位置是_______
(2)请写出该反应的化学方程式: ;
(3)曾利用铝和铁的氧化物反应原理来焊接钢轨,该反应的化学方程式为
(4)现有铁和铂组成的合金共a mol,其中Pt的物质的量分数为x,研成粉末状后全部投入含bmol HNO3的稀溶液中,使其充分反应,且HNO3的还原产物只有NO。试回答下列问题:
①随HNO3用量的增加,溶液中的金属离子和残留固体的成分依次有四种情况,请用粒子符号填写下表空白:
① | ② | ③ | ④ | |
溶液中的金属离子 | Fe2+ | |||
残留固体成分 | Fe、Pt | Pt | Pt |
②当x="0.5" ,且溶液中Fe3+与Fe2+和物质的量相等,在标准状况下共产生112mLNO。
则a = ,b = ,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)是一种具有许多优良性能的的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为_____________________。
②BH![]() 的空间构型是________________________________(用文字描述)。
的空间构型是________________________________(用文字描述)。
③与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有________种。
(2)二氧化钛(TiO2 )是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。
①纳米TiO2催化的一个实例如下图所示。
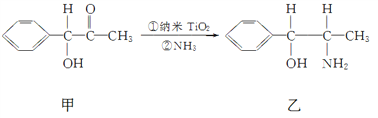
化合物甲的分子中采取sp2杂化方式的碳原子个数为________, 化合物乙中采取sp3杂化的原子的第一电离能由小到大的顺序为____________。
②在 TiO2催化作用下,可将CN- 氧化成CNO- ,进而得到N2 。与CNO- 互为等电子体的分子、离子化学式分别为_____________、_______________(各写一种)。
(3)金属钛内部原子的堆积方式与铜相同,都是面心立方堆积方式,如下图。若该晶胞的密度为ρ g·cm-3,阿伏加德罗常数为NA,则该晶胞的边长为________cm。
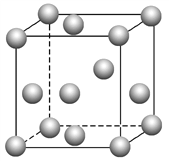
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见有机物间的转化关系如图所示(以下变化中,某些反应条件及产物未标明)。A是天然有机高分子化合物,D是一种重要的化工原料。在相同条件下,G蒸气密度是氢气的44倍。
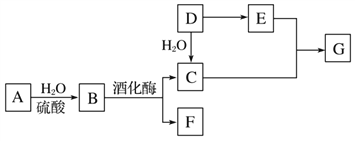
(1)D的名称:_____________。
(2)C和E反应的化学方程式:_____________________________________。
(3)检验A转化过程中有B生成,先中和水解液,再需要加入的试剂是_____________。
(4)某烃X的相对分子质量是D、F之和,分子中碳与氢的质量之比是5∶1。下列说法正确的是________(填字母)。
A.X 不溶于水,与苯互为同系物 B.X性质稳定,高温下不会分解
C.X的同分异构体可能存在4个甲基 D.X可能和溴水发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com