
 2 SO3 (g)�������������Ҫ��Ӧ֮һ���±���ԭ������V(SO2):V(O2):V(N2)=7:11:82Ͷ�ϣ���1��01��105Paʱ����ͬ�¶���SO2��ƽ��ת���ʡ�
2 SO3 (g)�������������Ҫ��Ӧ֮һ���±���ԭ������V(SO2):V(O2):V(N2)=7:11:82Ͷ�ϣ���1��01��105Paʱ����ͬ�¶���SO2��ƽ��ת���ʡ�| �¶�/�� | 400 | 500 | 600 |
| SO2ת����/% | 99��2 | 93��5 | 73��7 |

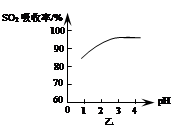
 H2SO3 MnO2+ H2SO3===MnSO4+H2O����MnO2+ SO2==MnSO4��
H2SO3 MnO2+ H2SO3===MnSO4+H2O����MnO2+ SO2==MnSO4�� H2SO3
H2SO3 H++������Һ��������ǿ��ƽ�������ƶ���ʹSO2����ϵ�������
H++������Һ��������ǿ��ƽ�������ƶ���ʹSO2����ϵ������� H2SO3 MnO2+ H2SO3= MnSO4+H2O��
H2SO3 MnO2+ H2SO3= MnSO4+H2O�� H2SO3
H2SO3 H++ HSO3-������Һ��������ǿ��ƽ�������ƶ���ʹ�����������ϵ���ݳ���
H++ HSO3-������Һ��������ǿ��ƽ�������ƶ���ʹ�����������ϵ���ݳ���


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
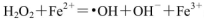
 ����Fe2���ڴ˹����������������______________��������336mL O2����״����ʱ����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ_______mol��
����Fe2���ڴ˹����������������______________��������336mL O2����״����ʱ����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ_______mol��
 .
.�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
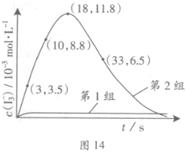
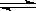 Z �ڷ�Ӧ�����еķ�Ӧ���ʣ�v����ʱ�䣨t���Ĺ�ϵ���ߣ�������������ȷ���� �� ��
Z �ڷ�Ӧ�����еķ�Ӧ���ʣ�v����ʱ�䣨t���Ĺ�ϵ���ߣ�������������ȷ���� �� �� 
| A��t1ʱ������Ӧ���ʴ����淴Ӧ���� |
| B��t2ʱ���ﵽ�������µ����Ӧ�� |
| C��t2- t3����Ӧ���ٷ����������ʵ�Ũ����� |
| D��t3�÷�Ӧ�ķ�Ӧ���п��ܱ���������ı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 x Q(g)+3R(g)����2min��ƽ�⣬����2.4molR�������Q��Ũ��Ϊ0.4mol/L����
x Q(g)+3R(g)����2min��ƽ�⣬����2.4molR�������Q��Ũ��Ϊ0.4mol/L�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
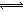 HOI(aq) ��H2
HOI(aq) ��H2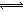 I2(aq)+H2O(l) ��H3
I2(aq)+H2O(l) ��H3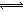 I3��(aq)����ƽ�ⳣ������ʽΪ_______��
I3��(aq)����ƽ�ⳣ������ʽΪ_______��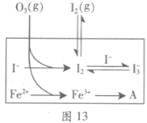
| ��� | ��Ӧ�� | ��ӦǰpH | ��Ӧ��pH |
| ��1�� | O3+ I�� | 5.2 | 11.0 |
| ��2�� | O3+ I��+ Fe2+ | 5.2 | 4.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����������ܺ� | B��ʹ��Ӧ��Ļ�ѧ�������ƻ� |
| C��ʹ��Ӧ����ȫ | D��ʹ��Ӧ�ų���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| | ��������ĩ״��/mol | ���Ũ�ȼ���� | ��Ӧ�¶� | ||
| A | Mg | 0.1 | 3mol��L-1���� | 10mL | 25�� |
| B | Fe | 0.1 | 3mol��L-1���� | 10mL | 25�� |
| C | Mg | 0.1 | 3mol��L-1���� | 10mL | 25�� |
| D | Mg | 0.1 | 6mol��L-1���� | 10mL | 60�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g)������������Ӧ���ʵĴ�ʩ�ǣ� ��
2SO3(g)������������Ӧ���ʵĴ�ʩ�ǣ� ��| A��ͨ�����O2 | B�����������ݻ� |
| C����ȥ����SO3 | D��������ϵ�¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com