
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )
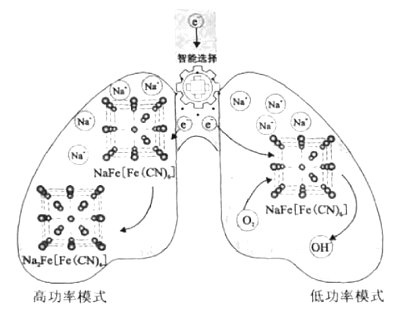
A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
【答案】D
【解析】
A.根据图示可知:电池以低功率模式工作时,负极是Zn-2e-=Zn2+,正极上是NaFe[Fe(CN)6]获得电子,然后与吸附在它上面的氧气即溶液中发生反应为O2+4e-+2H2O=4OH-,从NaFe[Fe(CN)6]上析出,故NaFe[Fe(CN)6]的作用是作催化剂,A正确;
B.电池以低功率模式工作时,电子进入NaFe[Fe(CN)6]时Na+的嵌入;当形成OH-从NaFe[Fe(CN)6]析出时,Na+从NaFe[Fe(CN)6]脱嵌,因此Na+的嵌入与脱嵌同时进行,B正确;
C.根据电池以高功率模式工作时,正极上NaFe[Fe(CN)6]获得电子被还原变为Na2Fe[Fe(CN)6],所以正极的电极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6],C正确;
D.若在无溶解氧的海水中,由于在低功率模式工作时需要氧气参与反应,因此在该电池不能实现长续航的需求,D错误;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】下列化学反应中,属于氧化还原反应的是( )
A.SO3 + H2O === H2SO4B.CaCO3 === CaO + CO2↑
C.Zn + H2SO4 === ZnSO4 + H2↑D.AgNO3 + NaCl![]() AgCl↓+ NaNO3
AgCl↓+ NaNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100mol·L-1NaOH溶液分别滴定20.00ml 0.100mol·L-1的盐酸和醋酸,滴定曲线如下图所示。下列说法正确的是( )

A. Ⅱ表示的是滴定醋酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)小于滴定盐酸消耗的V(NaOH)
C. V(NaOH)=10.00mL时,醋酸溶液中C(CH3COO-)+2C(H+)=C(CH3COOH)+2C(OH-)
D. V(NaOH)=20.00mL时,两份溶液中C(Cl-)=C(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出)。图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。
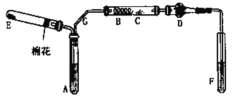
(1)为使A中乙醇平稳地汽化成乙醇蒸气,常采用的方法是_____________。
(2)若E中的固体为纯净物,则E的化学式是_____________。
(3)写出B处发生反应的化学方程式_____________
(4)加热F处的混合液的实验现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g) ![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 容器内压强不随时间变化B. 容器内,3种气体AB、A2、B2共存
C. 容器中各组分的体积分数不随时间变化D. AB的消耗速率等于A2的消耗速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10 ℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50 ℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
甲同学认为,该溶液的pH升高的原因是HCO3-水解程度增大,故碱性增强,该反应的离子方程式为_____。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3并推断Na2CO3的水解程度______NaHCO3 (填”大于”或”小于”)。丙同学认为甲、乙的判断都不充分。
丙认为: (1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则____(填”甲”或”乙”)判断正确。试剂X是____。
A.Ba(OH)2溶液 B.BaCl2溶液 C.AlCl3溶液 D.澄清石灰水
(2)查阅资料发现NaHCO3的分解温度为150℃,丙断言____(填”甲”或”乙”)的判断是错误的,理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得知,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+ = 2Mn2++10CO2↑+8H2O该组同学设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;请回答:
(1)将草酸晶体配制成溶液时,必须用到的玻璃仪器是烧杯、玻璃棒、_____、______。
(2)滴定时,将KMnO4标准液装在右图中的________(填“甲”或“乙”)滴定管中。
![]()
(3)本实验滴定达到终点的标志是________。
(4)通过上述数据,计算出x=________。
(5)下列滴定操作会使测得的x值偏大的是________。
A.滴定终点时俯视滴定管刻度
B. 滴定终点时仰视滴定管刻度
C.滴定时所用的KMnO4溶液因久置而导致浓度变小
D.滴定管尖嘴内在滴定前有气泡,滴定后气泡消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计如图装置,验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物(杂质不参与反应)。

回答下列问题。
(1)仪器a的名称______,碱石灰的作用______。
(2)为检验灼烧黄铜矿产生的气体,B中可选______
a.HNO3溶液b.品红溶液c.BaCl2溶液d.溴水e.酸性KMnO4溶液
(3)C中NaOH的作用______。
(4)样品经煅烧后的固体中铜元素以泡铜(Cu、Cu2O)形式存在,其中Cu2O能与稀硫酸反应生成Cu和CuSO4。
①设计实验验证泡铜中含有Cu2O:取少量泡铜置于试管中,________,若________,说明泡铜中含有Cu2O。
②用泡铜与CO反应来制取粗铜,再经精炼可得纯铜。将一定量的纯铜投入到2L1mol/L的稀硝酸中充分反应,请写出该反应的离子方程式_______。若铜全部溶解并得到标况下4.48LNO,要使溶液中的Cu2+恰好沉淀,需要向反应后的溶液中加入5mol/L的NaOH溶液____L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com