
【题目】乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得知,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+ = 2Mn2++10CO2↑+8H2O该组同学设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;请回答:
(1)将草酸晶体配制成溶液时,必须用到的玻璃仪器是烧杯、玻璃棒、_____、______。
(2)滴定时,将KMnO4标准液装在右图中的________(填“甲”或“乙”)滴定管中。
![]()
(3)本实验滴定达到终点的标志是________。
(4)通过上述数据,计算出x=________。
(5)下列滴定操作会使测得的x值偏大的是________。
A.滴定终点时俯视滴定管刻度
B. 滴定终点时仰视滴定管刻度
C.滴定时所用的KMnO4溶液因久置而导致浓度变小
D.滴定管尖嘴内在滴定前有气泡,滴定后气泡消失
【答案】100mL容量瓶 胶头滴管 甲 当最后一滴高锰酸钾滴入,溶液突然出现紫色(或紫红色),且半分钟内不褪色 2 A
【解析】
(1)配制100.00 mL一定物质的量浓度的草酸溶液,所需用到的玻璃仪器有烧杯、玻璃棒、100mL容量瓶、 胶头滴管,故答案为:100mL容量瓶、胶头滴管;
(2)因为KMnO4具有强氧化性,会腐蚀橡胶管,故应用酸式滴定管盛装,故答案为:甲;
(3)可利用KMnO4溶液自身的颜色作为指示剂判断滴定终点时,再滴加KMnO4溶液时,溶液将由无色变为紫色,故答案为:当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;
(4)设25mL草酸溶液中含草酸的物质的量为x mol,由题目所给化学方程式可知:
2MnO4-+ 6H+ + 5H2C2O4= 2Mn2++10CO2↑+8H2O
2 5
0.1000 mol/L×10.00 mL×10-3 L/mL x mol
x=(0.100 0 mol/L×10.00 mL×10-3 L/mL×5)/2=2.5×10-3 mol,
由此可计算出1.260g纯草酸晶体中含H2C2O4的物质的量为:
n(H2C2O4)=2.5×10-3 mol×(100 mL/25 mL)=0.0100 mol,
则1.260 g H2C2O4xH2O中含H2O的物质的量为:(1.260 g-0.0100 mol×90 g/mol)/18 g/mol=0.020 0 mol,计算可得:x=2。
(5)
A. 滴定终点时俯视滴定管刻度,则所读消耗酸性KMnO4溶液的体积偏小,由此计算所得n(H2C2O4)偏小,则n(H2O)偏大,x偏大;
B. 滴定终点时仰视滴定管刻度,则所读消耗酸性KMnO4溶液的体积偏大,由此计算所得n(H2C2O4)偏大,则n(H2O)偏小,x偏小;
C.滴定时所用的KMnO4溶液因久置而导致浓度变小,则消耗KMnO4溶液的体积偏大,由此计算所得n(H2C2O4)偏大,则n(H2O)偏小,x偏小;
D.滴定管尖嘴内在滴定前有气泡,滴定后气泡消失,则所读酸性KMnO4溶液的体积偏大,由此计算所得n(H2C2O4)偏大,则n(H2O)偏小,x偏小;
答案应选A。


科目:高中化学 来源: 题型:
【题目】在不同条件下进行合成氨的反应(N2+3H2![]() 2NH3),根据下列在相同时间内测定的正反应速率判断,生成NH3的速率最快的是
2NH3),根据下列在相同时间内测定的正反应速率判断,生成NH3的速率最快的是
A. v(H2)=0.3 mol·L-1·min-1 B. v(N2)=0.2 mol·L-1·min-1
C. v(NH3)=0.3 mol·L-1·min-1 D. v(H2)=0.005 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂碳、铝、铬是重要的元素,在工业生产和科技中有重要的应用。
(1)铝热反应可以冶炼金属铬,Cr基态核外电子排布式为_____________。
(2)金属锂是锂电池重要的组成部分。Li、Be、B 原子的第一电离能由大到小的顺序为______。
(3)LiAlH4是有机合成中常用的还原剂。AlH4-的空间构型为___________。
(4)![]() +
+
![]()
![]() +CH3COOH
+CH3COOH
①乙酸酐分子中碳原子轨道的杂化类型为________。
②l mol对甲基苯乙酮分子中含有的σ键的数目为_______
③甲苯分子难溶于水的原因是________。
(5)已知铬酸钙晶胞如图所示,该晶体密度为ρ g·cm-1,NA是阿伏加德罗常数的值。Ca离子周围距离最近且相等的O有_____个。相邻两个面心氧离子最短核间距(d)为_______pm。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )
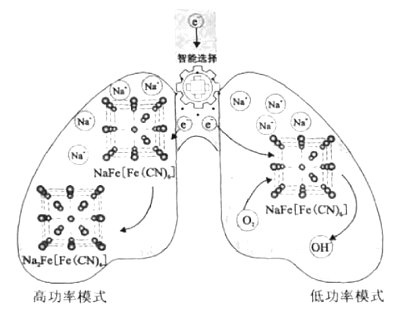
A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中非金属元素原子的电负性大小顺序是__。基态K+的电子排布式为__。
(2)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是__,中心原子的杂化方式为__。NaBH4中存在__(填标号)。
a.离子键 b.氢键 c.σ键 d.π键
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为__,其中Be的配位数为__。
(4)第三周期元素氟化物的熔点如下表:
化合物 | NaF | MgF2 | AlF3 | SiF4 | PF5 | SF6 |
熔点/℃ | 993 | 1261 | 1291 | -90 | -83 | -50.5 |
解释表中氟化物熔点变化的原因:___。
(5)CaF2的一种晶胞如图所示。Ca2+占据F-形成的空隙,若r(F-)=xpm,r(Ca2+)=ypm,设阿伏加德罗常数的值为NA,则CaF2的密度ρ=__g·cm-3(列出计算表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计了如图所示装置。

(1)a和b不连接时,烧杯中现象是__________________。
(2)a和b用导线连接,Cu极为原电池_____(“正”或“负”)极,电极反应式为____;溶液中H+移向_____(填“Cu”或“Zn”)极。电池总反应化学方程式为_______________。
(3)若电解质溶液改为AgNO3溶液,当转移0.2mol电子时,则理论上Cu片质量变化为_____。
II.某温度下,在2 L密闭容器中,X、Y、Z三种气态物质发生化学反应时,物质的量随时间变化的关系曲线如图所示:

(1)由图中的数据分析,该反应的化学方程式为__________________。
(2)5 min内用Z表示的平均反应速率为____________。
(3)化学反应速率受到很多因素的影响,例如:实验室制取氢气时一般用粗锌替代纯锌和稀硫酸反应,这是利用________________原理加快了氢气生成的速率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯分子结构的说法中,错误的是( )
A.各原子均位于同一平面上,6个碳原子彼此连接成为一个平面正六边形的结构
B.苯环中含有3个C—C单键,3个![]() 双键
双键
C.苯分子中6个碳碳键完全相同
D.苯分子中碳碳之间的键是介于单键和双键之间特殊的键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是我国学者研发的高效过氧化氢一尿素电池的原理装置:
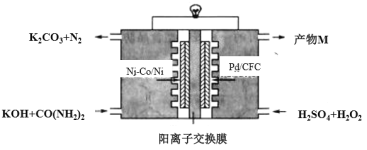
该装置工作时,下列说法错误的是
A.Ni-Co/Ni极上的电势比Pd/CFC极上的低
B.向正极迁移的主要是K+,产物M主要为K2SO4
C.负极反应为:CO(NH2)2+8OH–-6e–=CO32–+N2↑+6H2O
D.Pd/CFC极上发生反应:H2O2+2e–=2OH–
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如右所示。下列关于分枝酸的叙述正确的是( )

A. 可与乙醇、乙酸反应,且反应类型相同
B. 分子中含有2种官能团
C. 1mol分枝酸最多可与3mol NaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com