
【题目】如图所示,A处通入氯气,打开B阀时,C处红色布条不褪色;关闭B阀时,C处红色布条褪色;由此作出的判断正确的是( )
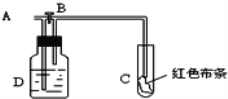
A. D中可能是浓硫酸
B. 通入的氯气含有水蒸气
C. D中可能是水
D. D中可能是NaOH溶液
【答案】C
【解析】从A处通入氯气,若打开活塞B,C处的有色布条不褪色,因为干燥的氯气不具备漂白性,若关闭活塞B,C处的有色布条褪色,这说明氯气经过溶液D后带出了水,潮湿的氯气具有漂白性;发生反应为Cl2+H2O=HCl+HClO;生成的次氯酸具有漂白作用。A、D中盛放浓硫酸时,具有吸水作用,关闭活塞B,C处的有色布条不会褪色,故A错误;B、A处通入的是潮湿的氯气时,具有漂白性,若打开活塞B,C处的有色布条会褪色,故B错误;C、D中盛放水时,氯气通过会带出水,潮湿的氯气具有漂白性,关闭活塞B,C处的有色布条褪色,故C正确;D、D盛放的是氢氧化钠溶液时,会和氯气发生反应,生成氯化钠、次氯酸钠和水,这样再关闭活塞B,C处的有色布条不会褪色,故D错误;故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:
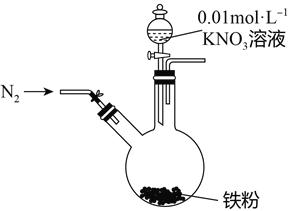
实验步骤 | 实验现象 |
1、打开弹簧夹,缓慢通入N2 | |
2、加入pH为2.5的0.01mol/L酸性KNO3溶液100mL | 铁粉部分溶解,溶液呈浅绿色; 铁粉不再溶解后,剩余铁粉表面出现少量白色物质附着。 |
3、反应停止后,拔掉橡胶塞,将圆底烧瓶取下 | 烧瓶内气体的颜色没有发生变化。 |
4、将剩余固体过滤 | 表面的白色物质变为红褐色。 |
(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是______________________________。
(2)白色物质是__________,用化学方程式解释其变为红褐色的原因:____________________。
(3)为了探宄滤液的成分,该同学进一步设计了下述实验:
实验步骤 | 实验现象 |
1、取部分滤液于试管中,向其中加入KSCN溶液 | 溶液液无变化 |
2、将上述溶液分为两份,一份中滴入氯气;另一份中滴加稀硫酸 | 两份溶液均变为红色 |
3、另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸。 | 有气体生成,该气体使红色石蕊试纸变蓝。 |
(i)根据以上实验现象,可以判断滤液中存在____________________离子。
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量KOH溶液,若氯气与KOH恰好完全反应,产物中可能有KCl、KClO、KClO3,且c(Cl-)/c(ClO-)的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )
A. 若某温度下,反应后c(Cl-)/c(ClO-)=11,则溶液中c(ClO-)/ c(ClO3-)=2: 1
B. 参加反应的氯气的物质的量等于a/2 mol
C. 改变温度,反应中转移电子的物质的量ne的范围:a/2mol≤ne≤5a/6 mol
D. 改变温度,产物中KClO3的最大理论产量为a/7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取氯化钠和碳酸钠的混合固体13.9g,加入50g水使其完全溶解,滴入90.5g稀盐酸恰好完全反应,反应后所得溶液质量为150g,请计算:
(1)完全反应后,生成CO2的质量为 g。
(2)混合物中碳酸钠的质量分数。
(3)反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl=2NaCl+CO2↑+H2O).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1mol/L的MOH溶液逐滴加入一定浓度的HA溶液滴加过程中,溶液的pH与滴入HA溶液的体积关系如图所示,当pH=8时MOH溶液恰好被中和。则下列说法错误的是
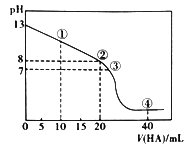
A. ②点混合溶液中水电离出的c(H+)大于HA溶液中由水电离出的c(H+)
B. ③点混合溶液中各离子浓度的大小关系是c(M+)=c(A-)>c(H+)=c(OH-)
C. 酸HA溶液的浓度为0.1mol/L
D. ④点溶液中,存在c(HA)+c(H+)>c(M+)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的量的计算
(1) 1mol HCl中含有HCl分子的个数是_______________________,1.204×1023个CH4分子的物质的量是____________mol。
(2)17克NH3的物质的量是 ______ mol,0.1mol H2O的质量是______________________g。
(3)标准状况下,11.2L O2的物质的量是 ______ mol ,1mol O2的体积是 ______ L。
(4)将8g NaOH配制成1L溶液,其物质的量浓度为_______________mol/L,1L 1mol/L NaOH溶液中含有溶质NaOH的质量是______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关纯碱和小苏打的叙述中正确的是 ( )
A. Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠溶液反应
B. 等质量Na2CO3、NaHCO3分别与相同浓度的盐酸反应,NaHCO3消耗的盐酸体积少
C. 向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀
D. 等物质的量Na2CO3、NaHCO3分别与足量稀H2SO4反应,NaHCO3产生的CO2多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 电解精炼铜,当外电路通过NA个电子时;阳极质量减少32 g
B. 反应3H2(g)+N2(g) ![]() 2NH3(g) △H=-92kJ·mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA
2NH3(g) △H=-92kJ·mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA
C. lmol·L-1的氯化铜溶液中,若Cl-的数目为2Na,则Cu2+的数目为Na
D. 标准状况下,NO和O2各11. 2L混合充分反应,所得气体的分子总数为0.75 Na
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com