
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 电解精炼铜,当外电路通过NA个电子时;阳极质量减少32 g
B. 反应3H2(g)+N2(g) ![]() 2NH3(g) △H=-92kJ·mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA
2NH3(g) △H=-92kJ·mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA
C. lmol·L-1的氯化铜溶液中,若Cl-的数目为2Na,则Cu2+的数目为Na
D. 标准状况下,NO和O2各11. 2L混合充分反应,所得气体的分子总数为0.75 Na
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图所示,A处通入氯气,打开B阀时,C处红色布条不褪色;关闭B阀时,C处红色布条褪色;由此作出的判断正确的是( )
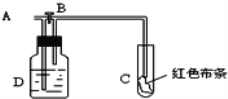
A. D中可能是浓硫酸
B. 通入的氯气含有水蒸气
C. D中可能是水
D. D中可能是NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—有机化学基础】有机物PAS-Na是一种治疗肺结核药物的有效成分,有机物G是一种食用香料,以甲苯为原料合成这两种物质的路线如下:


回答下列问题:
(1)![]() 生成A的反应类型是 。
生成A的反应类型是 。
(2)F中含氧官能团的名称是 ;试剂a的结构简式为 。
(3)写出由A生成B的化学方程式: 。
(4)质谱图显示试剂b的相对分子质量为58,分子中不含甲基,且为链状结构,写出肉桂酸与试剂b生成G的化学方程式:。
(5)当试剂d过量时,可以选用的试剂d是 (填字母序号)。
a.NaHCO3 b.NaOH c.Na2CO3
(6)写出C与足量NaOH在一定条件反应的化学方程式 。(不用写条件)
(7)肉桂酸有多种同分异构体,符合下列条件的有 种。
a.苯环上有三个取代基;
b.能发生银镜反应,且1mol该有机物最多生成4molAg。
由上述符合条件的同分异构体中,写出苯环上有两种不同化学环境氢原子的有机物的结构简式 (任写一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:
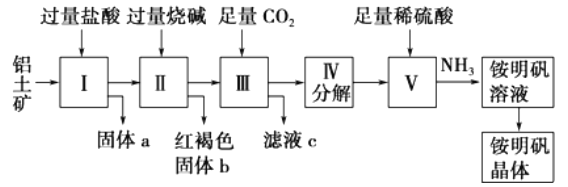
请回答下列问题:
(1)固体a的化学式为____,固体b化学式为____,Ⅲ中通入足量CO2气体发生反应的离子方程式为________________.
(2)由Ⅴ制取铵明矾溶液的化学方程式为______________.
(3)由I→II→III→IV都要用到的分离方法是______,由铵明矾溶液中制铵明矾晶体的操作是______________.
(4)如果先向铝土矿加入过量氢氧化钠,再加入过量盐酸,此时首先出现的固体a是__.
(5)向10gFe2O3、SiO2和Al2O3的混合物中,加入100ml稀硫酸,过滤后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示.则混合物中三氧化二铝的质量分数为______.
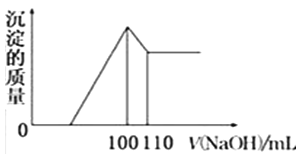
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关。下列各“剂”在应用过程中表现还原性的是( )
A. 臭氧柜里臭氧作餐具的“消毒剂” B. 热纯碱溶液常作厨房的“洗涤剂”
C. 活性铁粉在食品袋中作“去氧剂” D. 小苏打常作制糕点的“起泡剂”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气脱硝脱碳主要原理为:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0。在一定条件下的密闭容器中,用传感器测得该反应在不同时间NO和CO浓度如下表:
N2(g)+2CO2(g) △H<0。在一定条件下的密闭容器中,用传感器测得该反应在不同时间NO和CO浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 |
C(NO)/mol L-1 | 9.50×10-3 | 4.50×10-3 | 2.50×10-5 | 1.50×10-3 | 1.5×10-3 |
C(CO)/mol L-1 | 9.00×10-3 | 4.00×10-3 | 2. 00×10-3 | 1.00×10-3 | .1.00×10-3 |
下列说法正确的是
A. —定温度下,从开始到平衡,该反应的平衡常数逐渐增大
B. 前2s内的平均反应速率v(N2) = 1.75×10-3 mol·L-1·s-1
C. 达到平衡时,CO的转化率为11. 11%
D. 3s时NO和CO的浓度都不再变化,反应停止进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液,可能含有下列离子:Mg2+、A13+、Fe3+、Ba2+、H+、NH4+、SO42-、HCO3-、Cl-。取该溶液进行如下实验:①取溶液少许,滴入AgNO3溶液产生白色沉淀;②取溶液少许,滴入BaCl2溶液产生白色沉淀,加入足量稀硝酸沉淀不溶解;③取一定量的原溶液,加入一种淡黄色粉末状的固体X,产生气体的物质的量(n气体)、沉淀的物质的量(n沉淀)与加入淡黄色粉末的量(nx)的关系如下图所示(假设生成的气体全部逸出)。

根据实验现象和数据分析正确的是
A. 溶液中肯定大量存在的阳离子只有Mg2+、A13+、NH4+
B. 溶液中肯定没有的离子只有Fe3+、Ba2+
C. 当加入0.6mol淡黄色粉末时,生成两种气体分别为NH3和O2,其对应的体积比为2:3
D. 溶液中可能存在Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是

A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl-+ 2OH--2e-= ClO-+ H2O
C. 阴极的电极反应式为:2H2O + 2e-= H2↑ + 2OH-
D. 除去CN-的反应:2CN-+ 5ClO-+ 2H+= N2↑ + 2CO2↑ +5Cl-+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产、生活中有广泛应用,下列对应关系不正确的是
化学性质 | 实际应用 | |
A | SO2具有漂白性 | 用SO2漂白纸浆 |
B | Fe3+水解生成胶体 | 硫酸铁可用作净水剂 |
C | 维生素C易被氧气氧化 | 维生素C用作食品抗氧化剂 |
D | 硫酸是一种强酸 | 硫酸可用于除去锅炉中的水垢 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com