
【题目】接触法制硫酸的工业生产主要分为三步:第一步,矿石燃烧的设备叫_______,其中发生的主要反应式是_______;第二步制备三氧化硫的设备是_______,发生的主要化学反应方程式是:_______;第三步用_______而不用水吸收的主要原因是_______;最后的尾气中所含污染空气的主要有害物质是_______。
【答案】沸腾炉4FeS2+11O2![]() 2Fe2O3+8SO2接触室2SO2+O2
2Fe2O3+8SO2接触室2SO2+O2![]() 2SO398.3%的浓硫酸水吸收易形成酸雾阻止三氧化硫的吸收二氧化硫
2SO398.3%的浓硫酸水吸收易形成酸雾阻止三氧化硫的吸收二氧化硫
【解析】
第一步:工业制硫酸是利用黄铁矿在沸腾炉中燃烧生成二氧化硫,然后在接触室催化氧化二氧化硫得三氧化硫,最后吸收塔用98.3%的浓硫酸吸收SO3,其中黄铁矿燃烧反应方程式为4FeS2+11O2![]() 2Fe2O3+8SO2;第二步:接触室催化氧化,二氧化硫与空气中的氧气反应生成三氧化硫,则化学方程式为2SO2+O2
2Fe2O3+8SO2;第二步:接触室催化氧化,二氧化硫与空气中的氧气反应生成三氧化硫,则化学方程式为2SO2+O2![]() 2SO3;第三步:用98.3%的浓硫酸充分吸收SO3,为了防止形成酸雾,吸收塔中SO3如果用水吸收,发生反应SO3+H2O=H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍三氧化硫对水的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒98.3%的浓硫酸作吸收液,最终得到“发烟”硫酸,硫酸工厂排放的尾气中,含少量二氧化硫污染大气。
2SO3;第三步:用98.3%的浓硫酸充分吸收SO3,为了防止形成酸雾,吸收塔中SO3如果用水吸收,发生反应SO3+H2O=H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍三氧化硫对水的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒98.3%的浓硫酸作吸收液,最终得到“发烟”硫酸,硫酸工厂排放的尾气中,含少量二氧化硫污染大气。


科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:2SO2(g)+O2(g)═2SO3(g),△H<0.现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,按如图所示投料,并在400℃条件下开始反应.达到平衡时,下列说法正确的是( )

A. 容器Ⅰ、Ⅲ中平衡常数相同
B. 容器Ⅱ、Ⅲ中正反应速率相同
C. SO3的体积分数:Ⅱ<Ⅲ
D. 容器Ⅰ中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图制取SO2并验证SO2性质的装置图:
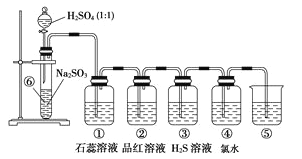
已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O。
(1)①中为紫色石蕊试液,实验现象为______,实验证明SO2是_______气体。
(2)②中为红色品红溶液,现象为______,证明SO2有_______性。
(3)④为紫红色高锰酸钾,实验现象为______,证明SO2有_______性。
(4)⑤的作用______,反应方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是一座巨大的化学资源宝库,从中可以提取许多常见的化学物质,结合所学知识回答下列问题,
(1)“吹出法”提溴空气吹出法是工业规模提溴的常用方法,其流程如下:

其中步骤②~④的目的是________________________________________________。步骤③反应的离子方程式为_______________________________________________。除SO2外,步骤③还可以选用Na2CO3溶液吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1molBr2时,转移电子的物质的量为__________________mol。
(2)实验室模拟从海带中提取碘,可能经历如下操作(或过程),请选择必要的操作(或过程),并按实验的先后顺序排列________________________________________________(填写编号)

仪器X的名称__________________,将X中的液体分离的具体操作为:打开X上端玻璃塞,_______________________________________________________________________________。
(3)卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子。现以卤块为原料按下图流程制备轻质氧化镁,若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,回答下列问题:

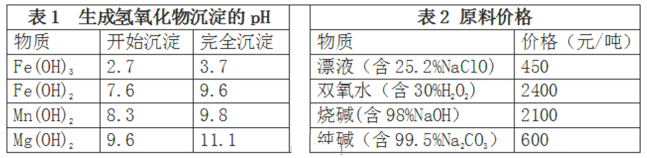
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去。
步骤①反应的离子方程式为:___________________________________________________;
步骤②的反应方程式为:_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中,可逆反应C(s)+CO2(g)![]() 2CO(g),达到平衡状态的标志是( )
2CO(g),达到平衡状态的标志是( )
①单位时间内生成n molCO2的同时生成n molC ②单位时间内生成n molCO2 的同时生成2n mol CO ③CO2 、CO的物质的量浓度之比为1: 2的状态 ④混合气体的密度不再改变的状态 ⑤混合气体的压强不再改变的状态 ⑥C的质量不再改变的状态
A. ①④⑤⑥ B. ②④⑤⑥ C. ②③⑤⑥ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为从海带中提取碘的工业生产过程,有关说法错误的是

A.因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘元素
B.碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀
C.在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等
D.在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为解决日益加剧的温室效应等问题,科学家正在研究建立如下图所示的二氧化碳新循环体系:
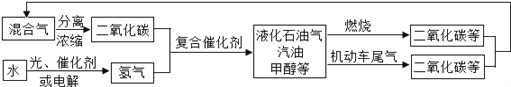
上述关系图能反映的化学观点或化学思想有:( )
①化学变化中元素种类是不变的;②燃烧时化学能可以转化为热能和光能;
③光能或电能可以转化为化学能;④无机物和有机物可以相互转化;
⑤二氧化碳可成为一种重要的资源。
A. ①②③④ B. ①②③⑤ C. ①②④⑤ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中粒子浓度关系正确的是( )
A. pH=1的NaHSO4溶液: c(H+)=c(SO![]() )+c(OH-)
)+c(OH-)
B. 含有AgCl和AgI固体的悬浊液: c(Ag+)>c(Cl-)=c(I-)
C. CO2的水溶液:c(H+)>c(HCO![]() )=2c(CO
)=2c(CO![]() )
)
D. 含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O![]() )+c(C2O
)+c(C2O![]() )+c(H2C2O4)]
)+c(H2C2O4)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:
A. 分子式为C7H8,分子中含有苯环的烃的一氯代物有4种
B. 硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
C. 如图所示实验可证明元素的非金属性:Cl>C>Si

D. C4H10的两种同分异构体因为分子间作用力大小不同,因而沸点正丁烷低于异丁烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com