
(经典回放)下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素.

(1)下列________(填写编号)组成元素的单质可能都是电的良导体.
①a、c、h
②b、g、k
③c、h、i
④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去.核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力
B.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
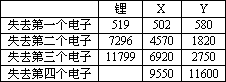
①通过上述信息和表中的数据分析为什么锂原子失去核外第2个电子所需的能量远远大于失去第1个电子所需的能量.________.
②表中X可能为以上13种元素中的________(填写字母)元素.用元素符号表示X和j形成化合物的化学式:________.
③Y是周期表中________族元素.
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需要的能量最多.
|
答案:(1)①④ (2)①Li原子失去一个电子后,Li+已形成稳定结构,此时再失去一个电子很困难 ②a Na2O和Na2O2 ③第ⅢA族 ④m 思路解析:本例实质上是考查电离能的知识.要弄清原子的各级电离能的变化有大突变和小突变,前者说明核外电子是分电子层排布的,后者则说明同一电子层的电子还处于不同的亚层(一种电子层). (1)金属是电的良导体,故应选①④. (2)①Li原子的结构示意图是Li ②X的第一电离能比锂小一些,说明失去电子比锂易,即比锂金属性更强一些,从表上看,应选钠,j是氧,钠与氧可生成氧化钠和过氧化钠. ③从Y的电离能数据可知第3和第4电离能之间有大突变,说明两者不在一个电子层;第1和第2电离能是小突变,说明它们不在同一亚层.即最外层有3个电子.在“ⅢA族或第3主族”. ④即第1电离能最大的应是稀有气体原子,应选m. |


科目:高中化学 来源: 题型:
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
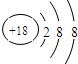
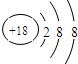


查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周 期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | E | F | H | J | ||||
| 3 | B | C | D | G | I |
查看答案和解析>>
科目:高中化学 来源: 题型:
(经典回放)下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
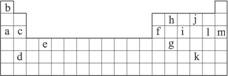
(1)下列________________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
①原子核对核外电子的吸引力
②形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1)
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | 9 550 | 11 600 |
通过上述信息和表中的数据分析锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量的原因。
____________________________________________________。
②表中X可能为以上13种元素中的(填写字母)元素。用元素符号表示X和j形成化合物的化学式____________________________________________________。
③Y是周期表中____________族元素。
④以上13种元素中____________(填写字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
科目:高中化学 来源: 题型:
(经典回放)下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
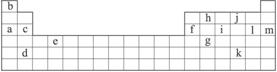
(1)下列____________(填写编号)组成元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、i ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力
B.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | 9 550 | 11 600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第2个电子所需的能量远远大于失去第1个电子所需的能量。_____________________________。
②表中X可能为以上13种元素中的_______________ (填写字母)元素。用元素符号表示X和j形成化合物的化学式:__________________。
③Y是周期表中_______________族元素。
④以上13种元素中,_______________(填写字母)元素原子失去核外第一个电子需要的能量最多。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com