
如图所示各为元素周期表的一部分,表中数字是原子序数,其中X为35的是
科目:高中化学 来源: 题型:
| ||
| 高温高压 |
| ||
| 高温高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示是前四周期的五种元素在周期表中的相对位置关系.乙和丁的原子序数之和为甲的4倍,则
如图所示是前四周期的五种元素在周期表中的相对位置关系.乙和丁的原子序数之和为甲的4倍,则查看答案和解析>>
科目:高中化学 来源: 题型:
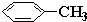
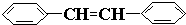
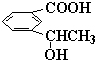

查看答案和解析>>
科目:高中化学 来源:河南省许昌高级中学2006~2007学年下学期期末教学质量评估试卷、高一化学 题型:022
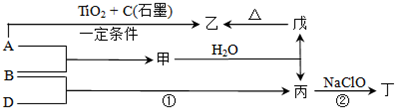
已知甲、乙、丙为常见单质,其中丙为气体,乙与丙的摩尔质量相同.A、B、C、D、X、Y、Z为常见化合物,Y的摩尔质量比Z的小16.各物质转化关系如图所示(各反应条件均已略去):

(1)写出B的电子式________,B中含有的化学键为________.
(2)用电子式表示X的形成过程:________________.
(3)与乙元素同周期的原子半径最小的元素W为________(填元素符号),写出W的单质与C在水溶液中反应的离子方程式:________________.
(4)若Y中含有Z,如何检验Z的存在?
________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:

请回答下列问题:
(1)写出Z的原子结构示意图_______________。
(2)写出图中D的电子式_______________。
(3)确定图中单质F的依据是_______________。
(4)利用图中反应③在标准状况下生成
(5)写出图中G溶液与H溶液相混合发生反应的离子方程式_______________。
(6)如下图所示装置,两玻璃管中盛有A饱和溶液,两极为多孔石墨电极,给两极分别通入X2、Z2气体,电流表的指针发生偏转;通入X2气体的电极名称是_______________(填写“正极”或“负极”);通入Z2气体的电极反应式为_______________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com