
| A、0.1 mol?L-1,pH=4 的 NaHB 溶液中:c(HB-)>c(H2B)>c(B2-) |
| B、10 mL 0.5 mol?L-1 CH3COONa 溶液与 6 mL 1 mol?L-1盐酸混合后的溶液中:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C、c(NH4+) 相等的 (NH4)2SO4溶液、(NH4)2CO3溶液和 NH4NO3溶液中:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4NO3) |
| D、NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |


科目:高中化学 来源: 题型:
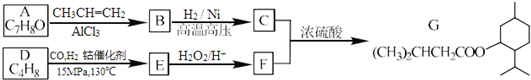
| 钴催化剂 |
| 15MPa,130℃ |
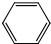 +CH2=CH2
+CH2=CH2| AlCl3 |

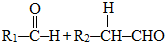
| 稀NaOH溶液 |
| △ |
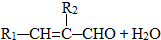
| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向苦卤中加入AgNO3,滤出沉淀,将溶液蒸干 |
| B、将苦卤蒸发浓缩,再加入AgNO3,把得到的溶液蒸发结晶 |
| C、给苦卤中加入熟石灰,分离出沉淀,用稀硝酸将沉淀溶解,再将溶液浓缩结晶 |
| D、将苦卤浓缩结晶,再进行电解,得到金属镁,用镁和HNO3反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(M+)>c(H+)>c(A-)>c(OH-) |
| B、c(M+)>c(A-)>c(OH-)>c(H+) |
| C、c(M+)>c(OH-)>c(A-)>c(H+) |
| D、c(M+)>c(A-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将蔗糖溶于水不能导电且其熔融状态也不能导电,故蔗糖不是电解质 |
| B、CO2溶于水得到的溶液能导电,所以CO2是电解质 |
| C、金属能导电,所以金属是电解质 |
| D、固态的NaCl不导电,所以 NaCl不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质B的质量分数增大了 |
| B、物质A的转化率减小了 |
| C、平衡向逆反应方向移动了 |
| D、a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、2:5 |
| C、1:2 | D、3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应属于氧化还原反应 |
| B、反应中NH3表现强氧化性 |
| C、生成28gN2有6mol电子转移 |
| D、反应后Cl2被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| D |
| ① |
| D |
| ② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com