
工业常用燃料与水蒸气反应制各H2和CO,再用H2和CO合成甲醇。
(1)制取H2和CO通常采用:C(s)+H2O(g)  CO(g)+H2(g) △H=+131.4kJ·mol-1,下列判断正确的是_______。
CO(g)+H2(g) △H=+131.4kJ·mol-1,下列判断正确的是_______。
A.该反应的反应物总能量小于生成物总能量
B.标准状况下,上述反应生成IL H2气体时吸收131.4kJ的热量
C.若CO(g)+H2(g)  C(s)+H2O(l) △H=-QkJ·mol-1,则Q<131.4
C(s)+H2O(l) △H=-QkJ·mol-1,则Q<131.4
D.若C(s)+CO2(g)  2CO(g) △H1;CO(g)+H2O(g)
2CO(g) △H1;CO(g)+H2O(g)  H2(g)+CO2(g) △H2 则:△H1+△H2=+131.4 kJ·mol-1
H2(g)+CO2(g) △H2 则:△H1+△H2=+131.4 kJ·mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO.该反应为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
己知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
不同时间各物质的物质的量/mol | ||||
0min | 2min | 4min | 6min | |
CH4 | 2.00 | 1.76 | 1.60 | n2 |
H2 | 0.00 | 0.72 | n1 | 1.20 |
根据表中数据计算:
①0min~2min内H2的平均反应速率为_______。
②达平衡时,CH4的转化率为________。在上述平衡体系中再充入2.00mol甲烷和1.00mol水蒸气,达到新平衡时H2的体积分数与原平衡相比______(填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有______(填字母)
A.CO的含量保持不变
B.容器中c(CH4)与c(CO)相等
C.容器中混合气体的密度保持不变
D.3v正(CH4)=v逆(H2)
( 3 )合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的。工作原理如下图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过)。

①a电极的名称为________。
②写出除去甲醇的离子方程式____________
 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:实验题
氢化钙固体是登山运动员常用的能源提供剂。某兴趣小组拟选用如下装置制备氢化钙。

请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为___ _____(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞;下一步操作是:_________(填序号)。
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此断,上述实验确有CaH2生成。
①写出CaH2与水反应的化学方程式______ ___________
②该同学的判断不正确,原因是______ ___________(用化学方程式表示)
(4)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附属中学高一上期中化学试卷(解析版) 题型:选择题
下列各种粒子,在氧化还原反应中通常只可作为氧化剂使用的是
A.SO32- B. MnO4- C.Cl- D.Fe
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江齐齐哈尔实验中学高一上期中化学卷(解析版) 题型:选择题
将一定体积密度为1.32g/cm3的硫酸溶液逐滴滴入到BaCl2溶液中,直到沉淀恰好完全为止。已知反应后所得溶液的质量等于原BaCl2溶液的质量,则原硫酸溶液浓度为( )
A.23.9% B.11.0% C.13.5mol/L D.5.67mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江齐齐哈尔实验中学高二上期中化学卷(解析版) 题型:选择题
常温下,pH=8的NaOH溶液与pH=10的KOH溶液等体积混合,溶液的c(H+)为
A.(10-8+10-10)/2 mol/L B.(10-8+10-10)mol/L
C.(10-14-5×10-5)mol/L D.2×10-10 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:实验题
有机物A 可由葡萄糖发酵得到,也可以从牛奶中提取。纯净的A 为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取A9.0g,升温其汽化,测其密度是相同条件下H2的45 倍. | 试通过计算填空: (1)A的相对分子质量为_______。 |
(2)将9.0gA在足量纯O2中充分燃烧,并使一其产物依次缓缓通过浓硫酸、碱石灰.发现两者分别增重5.4g和13.2g | (2)A的分子式为__________。 |
(3)另取A9.0g,跟足量的NaCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 | (3)写出A中所含官能团的名称______。 |
( 4 ) A 的核磁共振氢谱如下图: | ( 4 ) A中含有______种氢原子 |
(5)综上所述,A的结构简式为___________ | |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
分析下表中的四个热化学方程式,判断氢气和丙烷的标准燃烧热分别是
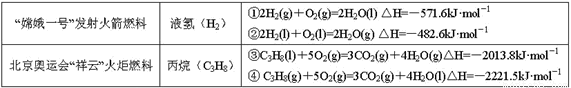
A.-571.6 kJ·mol-1,-2221.5 kJ·mol-1 B.-285.5 kJ·mol-1 ,-2013.8 kJ·mol-1
C.-285.8 kJ·mol-1,-2221.5 kJ·mol-1 D.-241.3 kJ·mol-1,-2013.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东枣庄八中南校区高二12月月考化学卷(解析版) 题型:选择题
25℃时,在10mL浓度均为0.1mol/LNaOH和NH3·H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是:
A.未加盐酸时:c(OH-)>c(Na+)= c(NH3·H2O)
B.入10mL盐酸时:c(NH4+) +c(H+) = c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
D.加入20mL盐酸时:c(Cl-) =c(NH4+) +c(Na+)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上期中测试化学试卷(解析版) 题型:选择题
下列关于胶体的叙述不正确的是
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间
B.一束光线透过胶体时,胶体中可发生丁达尔效应
C.胶体的分散质粒子直径比溶液的大,故胶粒不能透过滤纸
D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com