
分析下表中的四个热化学方程式,判断氢气和丙烷的标准燃烧热分别是
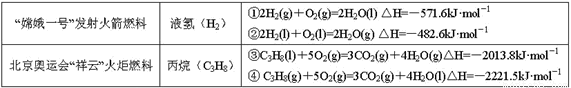
A.-571.6 kJ·mol-1,-2221.5 kJ·mol-1 B.-285.5 kJ·mol-1 ,-2013.8 kJ·mol-1
C.-285.8 kJ·mol-1,-2221.5 kJ·mol-1 D.-241.3 kJ·mol-1,-2013.8 kJ·mol-1
科目:高中化学 来源:2016届湖北武汉华中师大一附中等八校高三上联考一理化学卷解析版 题型:填空题
下图所示的四个容器中分别盛有不同的溶液,除a、b外,其余电极均为石墨电极。甲为铅蓄电池,其工作原理为:Pb+PbO2+2H2SO4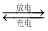 2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合K,发现g电极附近的溶液先变红,20min后,将K断开,此时c、d两极上产生的气体体积相同;据此回答:
2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合K,发现g电极附近的溶液先变红,20min后,将K断开,此时c、d两极上产生的气体体积相同;据此回答:
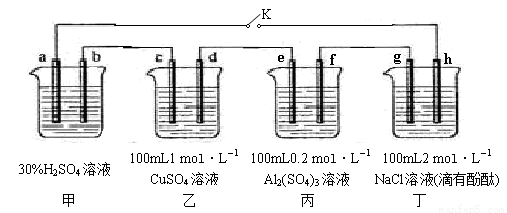
(1)a电极的电极材料是 (填“PbO2”或“Pb”)。
(2)丙装置中发生电解的总反应方程式为 。
(3)电解20min时,停止电解,此时要使乙中溶液恢复到原来的状态,需要加入的物质及其物质的量是 。
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连接上灵敏电流计,发现电流计指针偏转,则此时c电极为 极,d电极上发生反应的电极反应式为 。
(5)电解后取a mL丁装置中的溶液,向其中逐滴加入等物质的量浓度的CH3COOH溶液,当加入b mL CH3COOH溶液时,混合溶液的pH恰好等于7(体积变化忽略不计)。已知CH3COOH的电离平衡常数为1.75×10-5,则a/b = 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德市高二12月月考化学卷(解析版) 题型:选择题
高分子化合物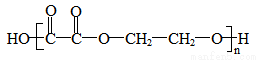 ,可由有机化工原料R和其他有机试剂,通过卤化、水解、氧化、缩聚反应得到,则R是( )
,可由有机化工原料R和其他有机试剂,通过卤化、水解、氧化、缩聚反应得到,则R是( )
A.1-丁烯 B.乙炔 C.1,3-丁二烯 D.乙烯
查看答案和解析>>
科目:高中化学 来源:2016届河北邯郸第一中学高三一轮收官考试一理综化学卷(解析版) 题型:填空题
工业常用燃料与水蒸气反应制各H2和CO,再用H2和CO合成甲醇。
(1)制取H2和CO通常采用:C(s)+H2O(g)  CO(g)+H2(g) △H=+131.4kJ·mol-1,下列判断正确的是_______。
CO(g)+H2(g) △H=+131.4kJ·mol-1,下列判断正确的是_______。
A.该反应的反应物总能量小于生成物总能量
B.标准状况下,上述反应生成IL H2气体时吸收131.4kJ的热量
C.若CO(g)+H2(g)  C(s)+H2O(l) △H=-QkJ·mol-1,则Q<131.4
C(s)+H2O(l) △H=-QkJ·mol-1,则Q<131.4
D.若C(s)+CO2(g)  2CO(g) △H1;CO(g)+H2O(g)
2CO(g) △H1;CO(g)+H2O(g)  H2(g)+CO2(g) △H2 则:△H1+△H2=+131.4 kJ·mol-1
H2(g)+CO2(g) △H2 则:△H1+△H2=+131.4 kJ·mol-1
(2)甲烷与水蒸气反应也可以生成H2和CO.该反应为:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
己知在某温度下2L的密闭绝热容器中充入2.00mol甲烷和1.00mol水蒸气,测得的数据如下表:
不同时间各物质的物质的量/mol | ||||
0min | 2min | 4min | 6min | |
CH4 | 2.00 | 1.76 | 1.60 | n2 |
H2 | 0.00 | 0.72 | n1 | 1.20 |
根据表中数据计算:
①0min~2min内H2的平均反应速率为_______。
②达平衡时,CH4的转化率为________。在上述平衡体系中再充入2.00mol甲烷和1.00mol水蒸气,达到新平衡时H2的体积分数与原平衡相比______(填“变大”、“变小”或“不变”),可判断该反应达到新平衡状态的标志有______(填字母)
A.CO的含量保持不变
B.容器中c(CH4)与c(CO)相等
C.容器中混合气体的密度保持不变
D.3v正(CH4)=v逆(H2)
( 3 )合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的。工作原理如下图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过)。

①a电极的名称为________。
②写出除去甲醇的离子方程式____________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
下列有关电解质溶液中微粒的物质的量浓度关系正确的是
A.在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3)
C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液pH=7,c(Na+)=0.1 mol·L-1:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上期中考试化学试卷(解析版) 题型:填空题
(1)请结合必要的方程式,尝试从微粒的电荷情况和电离平衡的移动两方面解释为什么碳酸的分步电离一步比一步困难?(请用方程式并结合必要的文字来回答该小题)
(2)某温度(t℃)时,测得0.01 mol·L-1 NaOH溶液的pH=13,请回答下列问题:
①该温度下水的Kw= 。
②此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va︰Vb= 。
(3)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;
H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11。某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于 _____ _____。
请设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论),要求仪器自选。
【供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸。】______ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东枣庄三中高二10月学情调查化学卷(解析版) 题型:选择题
根据下图,可判断出下列离子方程式中错误的是
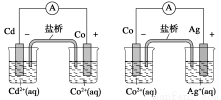
A.2Ag(s)+Cd2+(aq)===2Ag+(aq)+Cd(s)
B.Co2+(aq)+Cd(s)===Co(s)+Cd2+(aq)
C.2Ag+(aq)+Cd(s)===2Ag(s)+Cd2+(aq)
D.2Ag+(aq)+Co(s)===2Ag(s)+Co2+(aq)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南南阳第一中学高一上第二次月考化学卷(解析版) 题型:选择题
有FeO、Fe3O4的混合物若干克,在足量H2气流中加热充分反应,冷却后称得剩余固体全为铁单质,且比原混合物减轻了0.8g,将等质量的原混合物与硫酸反应,欲使之完全溶解,需0.5mol•L﹣1的硫酸的体积至少为( )
A.0.1L B.0.2L C.0.4L D.0.5L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第一次月考化学试卷(解析版) 题型:填空题
(1)现有①铁片 ②熔融NaCl ③稀氨水 ④CH3COOH ⑤酒精 ⑥稀盐酸 ⑦H2SO4 ⑧KOH ⑨蔗糖 ⑩H2CO3,其中属于非电解质的是 ,属于强电解质的是 ,属于弱电解质的是 (用序号填空),选择其中的一种弱电解质,写出其在水中的电离方程式 。
(2)实验室制取Fe(OH)3胶体的化学反应方程式可表示为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com