
【题目】下列说法正确的是( )
A.SO2能使FeCl3,KMnO4水溶液褪色
B.可以用澄清石灰水鉴别SO2和CO2
C.硫粉在过量的纯氧中燃烧可以生成SO3
D.少量SO2通过浓的CaCl2溶液能生成白色沉淀
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3++Fe3+。下列说法正确的是( )
A. Ce元素位于元素周期表第六周期第IIIB族
B. ![]() 、
、![]() 是同素异形体
是同素异形体
C. 铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2
D. 铈的原子核外有58个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是元素周期表的一部分,请回答下列问题。
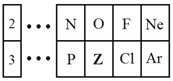
(1)Z元素在元素周期表中位于第________族。
(2)Z的原子半径__________(填“大于”、“小于”或“等于”)Si的原子半径。
(3)Cl元素的非金属性比Z元素的__________(填“强”或“弱”)。
(4)Z元素的气态氢化物的化学式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将两种不同物质的量浓度的Na2CO3溶液升高温度溶液中c(CO32-)变化如图所示,下列微粒的物质的量浓度关系正确的是( )
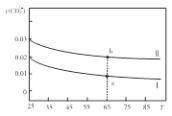
A.将溶液I升高温度,溶液pH减小
B.溶液a比溶液b中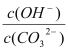 更大
更大
C.65℃时,向溶液a中加入1.06gNa2CO3固体,溶解后即为溶液b
D.溶液II一定存在:c(Na+)=2c(CO32-)+c(HCO3-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SOCl2(亚硫酰氯)是一种无色或淡黄色发烟液体,遇水或醇生成二氧化硫和氯化氢,用途非常广泛。已知:SO2+Cl2+SCl2=2SOCl2。
(1)SCl2的电子式为___________。
(2)上述SOCl2的制备反应中,生成1molSOCl2时转移________mol电子。
(3)SOCl2与足量NaHCO3溶液反应的离子方程式为____________。
(4)无水AlCl3是有机反应的催化剂,也是制取无水四氯铝酸锂(LiAlCl4)的原料,可由AlCl3溶液浓缩结晶得到AlCl3·6H2O,再脱水得到AlCl3。
①若将AlCl3溶液蒸发至干并充分灼烧,则最终得到的固体产物为___________(填化学式)。
②AlCl3·6H2O中加入SOCl2并加热可制得无水氯化铝,其反应化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
I.已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
2Fe(s)+3/2O2(g)=Fe2O3(s) △H=-825.5 kJ/mol
则反应:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) △H= kJ/mol。
2Fe(s)+3CO2(g) △H= kJ/mol。
II.反应1/3Fe2O3(s)+CO(g)![]() 2/3Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡。
2/3Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡。
(1)CO的平衡转化率= _____________。
(2)欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是________
a.提高反应温度 b.增大反应体系的压强
c.选取合适的催化剂 d.及时吸收或移出部分CO2
e.粉碎矿石,使其与平衡混合气体充分接触
III.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:CO(g)+ 2H2(g)![]() CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:
(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=________。
(2)若在一体积可变的密闭容器中充入l molCO、2molH2和1molCH3OH,达到平衡吋测得混合气体的密度是同温同压下起始的1.6倍,则该反应向________(填“正”、“逆”)反应方向移动。
(3)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
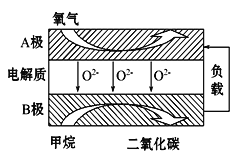
1)B极上的电极反应式为 。
2)若用该燃料电池做电源,用石墨做电极电解硫酸铜溶液,当阳极收集到11.2L(标准状况)气体时,消耗甲烷的体积为 L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳是引起“温室效应”的主要物质,应该减少二氧化碳的排放。
(1)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-a kJmol-1;
CH3OH(g)═CH3OH(l)△H=-b kJmol-1;
2H2(g)+O2(g)═2H2O(g)△H=-c kJmol-1;
H2O(g)═H2O(l)△H=-d kJmol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:_______________。
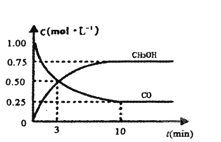
(2)在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H<0,测得CO2(g)和CH3OH(g)的浓度随时间变化如右图所示。
CH3OH(g)+H2O(g)△H<0,测得CO2(g)和CH3OH(g)的浓度随时间变化如右图所示。
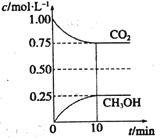
①从0min到10min,v(H2)=______。
②下列措施中能使![]() 增大的是______(选3填编号)。
增大的是______(选3填编号)。
A.升高温度 B.恒温恒容下充入He(g)
C.将H2O(g)从体系中分离 D.恒温恒容再充入2mol CO2和3mol H2
③计算该温度下此反应的平衡常数K=______(填分数或保留两位有效数字)。若改变______条件(填编号),可使K=1。
A.增大压强 B.增大反应物浓度 C.降低温度 D.升高温度 E.加入催化剂
(3)某甲醇燃料电池原理如图1所示
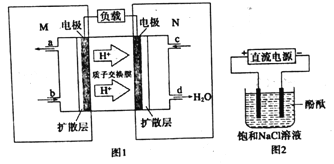
①则M区发生的电极反应式为______。
②用上述电池做电源,用图2装置电解饱和食盐水(电极均为惰性电极).则该电解反应的总反应的离子方程式为:__________________。
假设溶液体积为300mL,当溶液的pH值为13时(在室温下测定),理论上消耗甲醇的质量为______(忽略溶液体积变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下的定容密闭容器中,发生反应2SO2(g)+ O2(g) ![]() 2SO3(g), 下列哪种情况,能表明反应达到平衡状态
2SO3(g), 下列哪种情况,能表明反应达到平衡状态
A. SO3的体积百分含量保持不变
B. SO2速率是O2速率的2倍
C. SO3的浓度是O2浓度的2倍
D. 单位时间内SO2消耗的浓度等于SO3生成的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com