
(10分)现有下列仪器

(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室组成一套蒸馏装置肯定需要上述仪器中的一部分,按照实验仪器由下向上,从左到右的顺序,这些仪器依次是 ;还缺少的玻璃仪器是 (填仪器名称);仪器F的冷凝水应当从 口流出。
(2)海带等藻类物质经过处理后可以得到碘水,欲从碘水中提取碘需要上述仪器中的(填字母) ;该仪器名称为 ;向碘水中加入四氯化碳以提取碘单质的实验操作称为 ;静置分层后,单质碘主要溶解在 (填溶剂名称)中,该层此时的颜色为
科目:高中化学 来源:2015-2016学年北京大学附属中学分校高二上抽考化学试卷(解析版) 题型:选择题
下列有关中和热的说法正确的是
A.中和热的热化学方程式:H+(l)+OH-(l)===H2O(l) ΔH=-57.3kJ/mol
B.准确测量中和热的实验过程中,至少需测定温度4次
C.环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.若稀酸溶液中H+与稀碱溶液中OH-的物质的量相等,则所测中和热数值更准确
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东寿光中学高一上10月月考化学试卷(解析版) 题型:选择题
下列溶液中c(Cl-)与50mL 1mol/L 氯化铝溶液中的c(Cl-)相等的是
A.150 mL 1mol/L氯化钠溶液 B.75 mL 2mol/L氯化铵溶液
C.150 mL 1mol/L氯化铁溶液 D.75 mL 1mol/L氯化亚铁溶液
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第三次月考化学试卷(解析版) 题型:实验题
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献,他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:
NH3+CO2+H2O+NaCl NaHCO3↓+NH4Cl ;2NaHCO3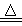 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
回答下列问题:
(1)氨气、二氧化碳与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
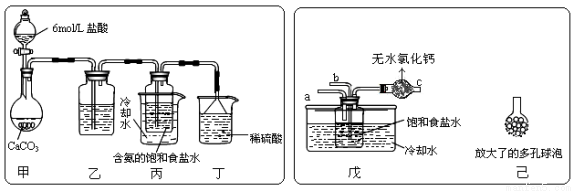
试回答下列有关问题:
 (Ⅰ)乙装置中的试剂是 ;
(Ⅰ)乙装置中的试剂是 ;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
②另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是 ;
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.NaAlO2溶液中通入过量CO2:2A1O2_+CO2+3H2O=2Al(OH)3↓+CO32-
B.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-=Na2SiO3↓ +H2O
C.向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2=I2+2H2O
D.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+ = H2O +BaCO3↓
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期中测试化学试卷(解析版) 题型:选择题
下列反应的离子方程式中正确的是
A.铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu
B.向氢氧化钡中滴加硫酸溶液H++OH﹣═H2O
C.Mg与盐酸的反应:2Mg+2H+═2Mg2++H2↑
D.石灰石与稀HCl反应制备CO2:CO32﹣+2H+═H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
CoCl3·4NH3用H2SO4溶液处理再结晶,SO42—可以取代化合物中的Cl—,但NH3的含量不变,用过量的AgNO3处理该化合物,有含量1/3氯以AgCl析出,这种化合物应该是
A.[Co(NH3)4] Cl3 B.[Co(NH3)4 Cl3]
C.[Co(NH3)4 Cl] Cl2 D.[Co(NH3)4 Cl2] Cl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上第一阶段测化学试卷(解析版) 题型:选择题
某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应A(g)+B(g)  C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
t/s | 0 | 5 | 15 | 25 | 35 |
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.反应在前5 s的平均速率v(A)=0.17 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,反应达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:选择题
下列溶液中导电性最强的是
A.1L0.1mol/L醋酸 B.0.1L 0.1mol/L H2SO4溶液
C.0.5L 0.1mol/L盐酸 D.2L 0.1mol/L H2SO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com