
下列反应的离子方程式中正确的是
A.铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu
B.向氢氧化钡中滴加硫酸溶液H++OH﹣═H2O
C.Mg与盐酸的反应:2Mg+2H+═2Mg2++H2↑
D.石灰石与稀HCl反应制备CO2:CO32﹣+2H+═H2O+CO2↑
科目:高中化学 来源:2015-2016学年辽宁育才学校高一上第一次阶段测化学试卷(解析版) 题型:选择题
(5分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法
B.加热分解
C.结晶法
D.分液法
E.蒸馏法
F.过滤法
(1) 分离饱和食盐水和沙子的混合物;
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(3) 分离水和油的混合物;
(4) 分离CCl4(沸点:76.75℃)和甲苯(沸点:110.6℃)的混合;
(5) 从碘的水溶液中提取碘。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期四调考试化学试卷(解析版) 题型:选择题
工业上常用电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是
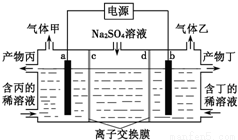
A.a极与电源的负极相连
B.产物丙为硫酸溶液
C.离子交换膜d为阴离子交换膜
D.a电极反应式:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第三次月考化学试卷(解析版) 题型:选择题
镁、铁混合物13.4g溶解在足量的稀硝酸中,完全反应得到还原产物只有6.72L(标况下)NO,则向反应后的溶液中加人足量的NaOH溶液,可生成的沉淀质量为
A.26.8 g B.28.7 g C.29.1 g D.29.5g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期中测试化学试卷(解析版) 题型:填空题
(10分)现有下列仪器

(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室组成一套蒸馏装置肯定需要上述仪器中的一部分,按照实验仪器由下向上,从左到右的顺序,这些仪器依次是 ;还缺少的玻璃仪器是 (填仪器名称);仪器F的冷凝水应当从 口流出。
(2)海带等藻类物质经过处理后可以得到碘水,欲从碘水中提取碘需要上述仪器中的(填字母) ;该仪器名称为 ;向碘水中加入四氯化碳以提取碘单质的实验操作称为 ;静置分层后,单质碘主要溶解在 (填溶剂名称)中,该层此时的颜色为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期中测试化学试卷(解析版) 题型:选择题
下列对摩尔的叙述中不正确的是
A.摩尔是一个单位,用于计量物质所含微观粒子的数量
B.摩尔是一个物理量
C.1mol任何气体所含的气体分子数目都相等
D.摩尔既能用来计量纯净物,又能用来计量混合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏拉萨中学高二上第一次月考化学试卷(解析版) 题型:填空题
(1)CH3-CH3→CH2=CH2+H2,有关化学键的键能如下:
化学键 | C-H | C=C | C-C | H-H |
键能(kJ/mol) | 414.4 | 615.3 | 347.4 | 435.3 |
计算该反应的反应热 (写出计算过程)
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
(3)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试计算1 mol肼和二氧化氮完全反应时放出的热量为__________________kJ,写出肼与二氧化氮反应的热化学方程式:______________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上第一阶段测化学试卷(解析版) 题型:选择题
在298K、101kPa时,已知:
(1)2H2O(g)= O2(g)+2H2(g) ΔH1
(2)Cl2(g)+H2(g)=2HCl(g) ΔH2
(3)2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是
A.ΔH3=ΔH1+2ΔH2 B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2 D.ΔH3=ΔH1-ΔH2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃兰州一中高二上期中测试文科化学试卷(解析版) 题型:填空题
(14分)在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+ O2 (g) 2SO3(g),△H<0
2SO3(g),△H<0
(1)写出该反应的化学平衡常数表达式K= 。
(2)降低温度,该反应K值 ,二氧化硫转化率 ,化学反应速度 (以上均填增大、减小或不变)
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是 。
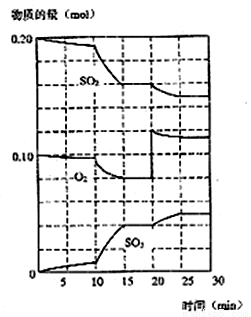
(4)据图判断,反应进行至20min时,曲线发生变化的原因是 (用文字表达)。10min到15min的曲线变化的原因可能是 (填写编号)。
a.加了催化剂 b.缩小容器体积
c.降低温度 d.增加SO3的物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com