
硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2。850℃~950℃时,硫铁矿在空气中煅烧,可能发生下列反应(设空气中N2与O2体积比为4∶1):
3FeS2 + 8O2 = Fe3O4 + 6SO2 ①
4FeS2 + 11O2 = 2Fe2O3 + 8SO2 ②
(1)含硫35%的硫铁矿样品(杂质不含硫),其FeS2的含量为_________________。
(2)设1 t纯净的FeS2按②式完全反应,产生标准状况下SO2__________ m3。
(3)为使FeS2煅烧完全生成Fe2O3,工业上使用过量空气,当空气过量20%时,所得炉气中SO2的体积分数为多少? 。
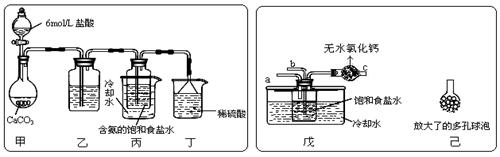
 (4)480 g纯净的FeS2在空气中完全反应,若所得固体中,
(4)480 g纯净的FeS2在空气中完全反应,若所得固体中,
 Fe和O的物质的量之比n(Fe)∶n(O) =4∶a,
Fe和O的物质的量之比n(Fe)∶n(O) =4∶a,
此时消耗空气为bmol。
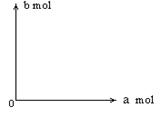
①试写出b与a的关系式:___________________。
②并作出b与a的关系曲线。
科目:高中化学 来源: 题型:
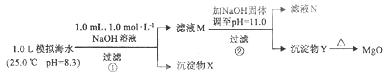
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
|
| Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0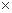 10-5mol
10-5mol L,可认为该离子不存在:
L,可认为该离子不存在:
实验过程中,假设溶液体积不变
Kkp,CaCo3=4.96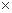 10-9 Kkp,MgCO3=6.82
10-9 Kkp,MgCO3=6.82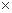 10-6
10-6
Kkp,Ca(OH)2=4.68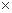 10-9 Kkp,Mg(OH)2=5.61
10-9 Kkp,Mg(OH)2=5.61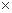 10-12
10-12
下列说法正确的是
A.沉淀物x为CaCO3
B.滤液M中存在Mg2+ ,不存在Ca2+
C.滤液N中存在Mg2+ , Ca2+
D.步骤②中应改为加入4.2g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
根据原子结构及元素周期律的知识,下列推断正确的是
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B、核外电子排布相同的微粒化学性质也相同 |
| C、Cl-、S2-、Na+、K+半径逐渐减小 |
| D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作、现象和解释或结论都正确的( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| ① | 过量的 | 溶液呈红色 | 稀 |
| ② | AgI沉淀中滴入稀 | 有白色沉淀出现 |
|
| ③ | Al箔插入稀 | 无现象 |
|
| ④ | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| ⑤ | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| ⑥ | 将足量的 |
| 2MnO4-+7H2O2+6H+=2Mn2++6O2↑+10H2O |
| ⑦ | 将一小块 | 产生气泡 |
|
| ⑧ | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下反应 |
A.①④⑤⑥⑦ B.④⑤ C.④⑤⑦ D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
(1)4FeO·Cr2O3 + 8Na2CO3 + 7O2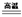 8Na2CrO4 + 2Fe2O3 + 8CO2
8Na2CrO4 + 2Fe2O3 + 8CO2
(2)2Na2CrO4 + H2SO4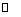 Na2SO4 + Na2Cr2O7 + H2O
Na2SO4 + Na2Cr2O7 + H2O
下列说法正确的是( )
A.反应(1)和(2)均为氧化还原反应
B.反应(1)的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4
D.反应(1)中每生成1molNa2CrO4时电子转移3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的数值,下列说法中正确的是( )
A. 1mol·L-1NaCl溶液含有NA个Na+离子
B. 常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.3NA
C. 盛有CO2的密闭容器中含有NA个氧原子,则CO2的物质的量不一定是0.5mol
D. 常温常压下,氧气和臭氧的混合物16g中含有NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
物质在相互反应时( )。
A.它们的质量一定相等
B.它们的物质的量一定相等
C.它们的质量比等于方程式中化学计量数之比
D.它们的物质的量之比等于方程式中化学计量数之比
查看答案和解析>>
科目:高中化学 来源: 题型:
随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。下列有关说法中正确的是
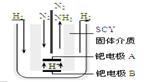 A.电解法合成氨的电解池中能用水作电解质溶液的溶剂
A.电解法合成氨的电解池中能用水作电解质溶液的溶剂
B.钯电极B连接的是电源的负极
C.钯电极A的电极反应式为:N2+6e—+6H+==2NH3
D.当有0.3mol电子转移时,有2.688L NH3生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com