
【题目】将一小块钠投入盛5 mLFeCl2的试管里,不可能观察到的现象是
A.钠熔成小球并在液面上游动
B.有无色无味的气体生成
C.溶液底部有银白色物质生成
D.溶液中产生的沉淀最终为红褐色
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法正确的是
A.2.4g金属镁所含电子数目为0.2NAB.16g CH4所含原子数目为NA
C.17gNH3所含中子数目为10 NAD.20g重水(D2O)所含质子数目为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。
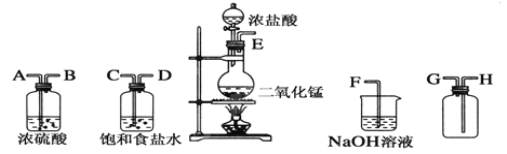
(1)连接上述仪器的正确顺序(填各接口处的字母):E接________;__________接__________;________接________;__________接F。
(2)装置中,饱和食盐水的作用是_____________________________________;浓硫酸的作用是________________________________________________。
(3)化学实验中检验是否有Cl2产生的常用方法是_________________________。
(4)写出下列反应的化学方程式:
①气体发生装置中的反应:_____________________________________。
②NaOH溶液中发生的反应:________________________________________。
(5)工业上用氯气制取漂白粉的化学反应方程式为__________________,漂白粉用于漂白、杀菌的原理用化学方程式表示为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用固体硫酸亚铁制取颜料铁红(Fe2O3)反应原理是:2FeSO4![]() Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有A、B、C三个装置。
Fe2O3+SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,依次将气体通过盛有A、B、C三个装置。

(1)B中盛放的溶液可以是_________________。
(2)A中放冰的作用是_______________________。
(3)设计一个简单的实验方案探究A中得到的沉淀的成分。___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物N是一种用于合成γ-分泌调节剂的药物中间体,其合成路线流程图如下:

(1)H的结构简式为______________________。
(2)下列有关说法错误的是________________。
A.G在一定条件下既能与酸反应,又能与碱反应
B. C能发生银镜反应
C.F→G的反应类型是取代反应
D.有机物N的分子式为C13H15NO5
(3)写出D→E的化学方程式:_________________________。
(4)写出同时满足下列条件的G的所有同分异构体的结构简式:____________________。
①含有苯环,核磁共振显示分子中只有四类氢
②能发生水解反应,且1mol该物质与NaOH溶液反应时最多可消耗2molNaOH
(5)丙烯A经过加成、氧化两步反应可合成C,请写出其合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是:
A. 将铜丝插入稀硝酸中:Cu+4H++2NO![]() ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B. 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe===2Fe2+
C. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH![]()
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学应用广泛。请回答下列问题:
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2Cu+2H2SO4+O2= 2CuSO4+2H2O,该电池的负极材料为_________;正极的电极反应式为__________________。
(2)燃料电池和二次电池的应用非常广泛。
①如图为甲烷燃料电池的示意图,电池工作时,b极的电极名称为_______;负极的电极反应式为____________;

②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2 + Pb+ 2H2SO4 === PbSO4 + 2H2O,铅蓄电池负极的电极反应式为__________;充电时,铅蓄电池的PbO2极应与外加直流电源的__极相连,PbO2极的电极反应式为_________。
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应质)时,以硫酸铜溶液为电解质溶液,粗铜做_____极;精炼一段时间后,当阴极增重128 g时,铅蓄电池参加反应的硫酸的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下的可逆反应CO(g)+2H2(g)![]() CH3OH(g) △H <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )
CH3OH(g) △H <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )

A. 温度:T1 < T2 3
B. 正反应速率:ν(a)>ν(c); ν(b)>ν(d)
C. 平衡常数: K(a) =K(c) ; K(b) >K(d)
D. 平均摩尔质量:M(a)<m(c); m(b)>M(d)</m(c); m(b)>
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铝的叙述中,不正确的是( )
A. 铝是地壳里含量最多的金属元素
B. 在常温下,铝不能与氧气反应
C. 铝是一种比较活泼的金属
D. 在化学反应中,铝容易失去电子,是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com