
| A、0.1 mol?L-1的NH4Cl溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B、0.1 mol?L-1的CH3COONa溶液中:c(OH-)=c(H+)+c(CH3COOH) |
| C、0.1 mol?L-1的Na2S溶液中:c(Na+)=2[c(HS-)+c(S2-)+c(H2S)] |
| D、pH=2的盐酸与pH=12的氨水等体积混合后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
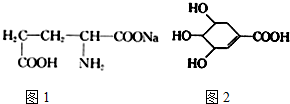
查看答案和解析>>
科目:高中化学 来源: 题型:
 )与P(
)与P( ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )| A、二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3:2 |
| B、二者在NaOH醇溶液中均可发生消去反应 |
| C、一定条件下,二者在NaOH溶液中均可发生取代反应 |
| D、Q的一氯代物只有1种、P的一溴代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它的单体的结构简式为:CH2=CH-COOR |
| B、它在一定条件下能发生加成反应 |
| C、它在一定条件下能发生缩聚反应 |
| D、它有固定的熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电解过程中,铜电极上有H2产生 | ||||
B、电解初期,总反应方程式为Cu+H2SO4
| ||||
| C、电解一定时间后,石墨电极上有铜析出 | ||||
| D、整个电解过程中,溶液pH值会增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在Si晶体中,Si原子与Si-Si键之比为1:4 |
| B、在NaCl晶体中,每个Na+周围距离最近的Na+有6个 |
| C、在CsCl晶体中,与每个Cs+紧邻的Cs+有8个 |
| D、在面心立方堆积的金属晶体中,每个金属原子周围紧邻的有12个金属原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com