
| Ԫ�ر�� | Ԫ��������ԭ�ӣ�����ӣ��ṹ |
| T | �����������Ǵ�����������3�� |
| X | �����µ��ʷ���Ϊ˫ԭ�ӷ��ӣ������к���3�Թ��õ��Ӷ� |
| Y | M���K����1������ |
| Z | ��������Ԫ�صĽ��������а뾶��С |
 ��
�� ��
�� ���� TԪ��ԭ�������������Ǵ�����������3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����TΪOԪ�أ�������X�ĵ���Ϊ˫ԭ�ӷ��ӣ������к���3�Թ��õ��Ӷԣ���XΪNԪ�أ�YԪ��ԭ��M���K����1�����ӣ���M�������Ϊ1����YΪNa����������Ԫ�صļ�������Z�İ뾶��С����ZΪAl���ݴ˽��
��� �⣺TԪ��ԭ�������������Ǵ�����������3����ԭ��ֻ����2�����Ӳ㣬����������Ϊ6����TΪOԪ�أ�������X�ĵ���Ϊ˫ԭ�ӷ��ӣ������к���3�Թ��õ��Ӷԣ���XΪNԪ�أ�YԪ��ԭ��M���K����1�����ӣ���M�������Ϊ1����YΪNa����������Ԫ�صļ�������Z�İ뾶��С����ZΪAl��
��1��TΪOԪ�أ�ԭ�ӽṹʾ��ͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��Na��Alͬ���ڣ���ԭ�������������Լ�������Na�Ľ����Խ�ǿ��
a�����ʵ��۵������������ʣ����ܱȽϽ�����ǿ������a����
b��������ǿ����ʧȥ���������йأ���ʧȥ������Ŀ�����أ����뻯�ϼ۸ߵ��أ���b����
c��Na������ˮ��Ӧ��Al���ʾ��ң�˵��Na�����Ը�ǿ����c��ȷ��
d��Na����������ˮ����ļ��Ա�Alǿ��˵���ƵĽ����Ը�ǿ����d��ȷ��
�ʴ�Ϊ��Na��cd��
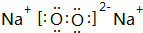
��3��O��N��Na��Al��������Ԫ�����γɼ������Ӽ����й��ۼ��Ļ�����û�����ΪNa2O2�������ʽΪ ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ѶȲ���ע���Ԫ�������ɵ��������գ�ע���������ս����ԡ��ǽ�����ǿ���Ƚ�ʵ����ʵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μ�����1.0mol/L HCl��Һ��ƽ�����淴Ӧ�����ƶ�����Һ��c��H+������ | |
| B�� | ��ˮ����Һ��c��H+����c��A-����c��HA��Ũ�Ⱦ���С | |
| C�� | ��������NaA���壬ƽ�����淴Ӧ�����ƶ�����Һ��c��H+������ | |
| D�� | ��������NaOH���壬ƽ��������Ӧ�����ƶ�����Һ��c��H+������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1���������顱������Ľᾧˮ�����һ�־��壬�þ�����ƽ��ÿ46��ˮ���ӹ���8������ÿ����������һ��������ӻ�һ������ˮ���ӣ����þ�����ÿ8����ֻ��6�����ɼ�����ӣ�����2��������ˮ������䣬�����顱ƽ����ɿɱ�ʾΪB������ţ���
��1���������顱������Ľᾧˮ�����һ�־��壬�þ�����ƽ��ÿ46��ˮ���ӹ���8������ÿ����������һ��������ӻ�һ������ˮ���ӣ����þ�����ÿ8����ֻ��6�����ɼ�����ӣ�����2��������ˮ������䣬�����顱ƽ����ɿɱ�ʾΪB������ţ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu2+��SO42-��Cl-��Na+ | B�� | OH-��K+��NO3-��Ba2+ | ||
| C�� | Na+��CO32-��Ca2+��Cl- | D�� | Mg2+��SO42-��Al3+��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Fe��NO3��3 ��Һ�е���������HI��Һ��2Fe3++2I-�T2Fe2++I2 | |
| B�� | ��AlCl3 ��Һ�м���������ˮ��Al3++3OH-�TAl��OH��3�� | |
| C�� | Cu��OH��2�������ڰ�ˮ�õ�����ɫ��Һ��Cu��OH��2+4NH3•H2O�T[Cu��NH3��4]2++2OH-+4H2O | |
| D�� | ����ʯ��ˮ�м�������NaHCO3 ��Һ��Ca2++2OH-+2HCO3-�TCaCO3��+CO32-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�2.24LSO3���еķ���������0.1NA | |
| B�� | 1 mol Na2O2������������Ϊ2NA | |
| C�� | ���³�ѹ�£�16gO2 ��O3�Ļ�����庬�е���ԭ����ΪNA | |
| D�� | ���³�ѹ���������£�33.6 LCl2��3.0g H2��Ӧ�����ɵ�HCl������ĿΪ3NA |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com