
CO2、CH4、BF3都是非极性分子,HF、H2O、NH3都是极性分子,由此推测ABn型分子是非极性分子的经验规律正确的是( )。
A.所有原子在同一平面
B.分子中每个键的键长应相等
C.在ABn中A原子没有孤对电子
D.A的相对原子质量小于B
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源:2014年高考化学 题型八 能量变化型专题练习卷(解析版) 题型:选择题
我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其它材料电池。电池总反应为V2O4+xLi LixV2O4下列说法正确的是( )
LixV2O4下列说法正确的是( )
A.该电池充电时锂极与外电源的负极相连
B.电池在放电时,Li+向负极移动
C.该电池充电时阴极的反应为LixV2O4-xe-=V2O4+xLi+
D.若放电时转移0.2 mol电子,则用去的锂为1.4x g
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型三 NA应用型专题练习卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列说法中正确的是( )
A.84 g NaHCO3晶体中含有NA个CO32-
B.9.2 g NO2和N2O4的混合气中含有的氮原子数为0.2NA
C.标准状况下,11.2 L臭氧中含NA个氧原子
D.78 g Na2O2与足量的CO2反应,电子转移个数为2NA
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型一 化学社会型专题练习卷(解析版) 题型:选择题
化学在生产和日常生活中有着重要的应用。下列叙述正确的是( )
A.在有机化工中,氯气是合成塑料、橡胶、人造纤维、农药、染料和药品的重要原料
B.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料
C.白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
D.汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科选修3化学训练2.2.2分子空间构型分子性质练习卷(解析版) 题型:填空题
元素X和Y属于同一主族。负二价的元素X和氢的化合物在通常状况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物,在这两种化合物中,X的质量分数分别为50%和60%。
(1)确定X、Y两种元素在周期表中的位置。X:____________;Y:____________。
(2)在X和Y两种元素形成的化合物中,写出X的质量分数为50%的化合物的化学式____________;该分子是____________(填“极性”或“非极性”)分子,分子构型为____________。
(3)写出X的质量分数为60%的化合物的化学式________;该分子中,中心原子以________杂化,是____________(填“极性”或“非极性”)分子,分子构型为____________。
(4)由氢、X、Y三种元素形成的常见化合物有两种,其水溶液均呈酸性,试分别写出其分子式____________、____________,并比较酸性强弱____________。
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科选修3化学训练1.2.2核外电子排布元素周期表练习卷(解析版) 题型:简答题
由下列元素在周期表中的位置,写出元素原子的价电子排布式。
(1)第4周期ⅥB族;
(2)第5周期ⅠB族;
(3)第5周期ⅣA族;
(4)第6周期ⅡA族;
(5)第4周期ⅦA族。
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科选修3化学训练1.2.2核外电子排布元素周期表练习卷(解析版) 题型:选择题
下列表示式错误的是( )。
A.Na+的轨道表示式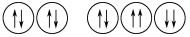
B.Na+的结构示意图: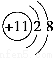
C.Na的电子排布式:1s22s22p63s1
D.Na的简化电子排布式:[Ne]3s1
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练3章物质聚集状态物质性质练习卷(解析版) 题型:填空题
Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
元素 | Mn | Fe | |
电离能 /kJ·mol-1 | I1 | 717 | 759 |
I2 | 1 509 | 1 561 | |
I3 | 3 248 | 2 957 | |
回答下列问题:
(1)Mn元素基态原子的价电子排布式为________,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是____________________________________________________________。
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。与Fe原子或离子形成配合物的分子或离子应具备的结构特征是________;②六氰合亚铁离子[Fe(CN)64-]中的配体CN-中C原子的杂化轨道类型是________,写出一种与CN-互为等电子体的单质分子的结构式________。
(3)三氯化铁常温下为固体,熔点282 ℃,沸点315 ℃,在300 ℃以上易升华。据此判断三氯化铁晶体为________。
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为________。
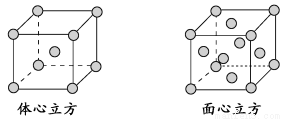
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练2.3离子键配位键与金属键练习卷(解析版) 题型:选择题
具有下列电子排布的原子中最难形成离子键的是( )。
A.1s22s22p2 B.1s22s22p5
C.1s22s22p63s2 D.1s22s22p63s1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com