
 、O:2s22p4、Na:
、O:2s22p4、Na:
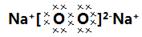 、2:1;
、2:1; 2Al2O3+3TiC
2Al2O3+3TiC 。氧原子的价电子的电子排布式为2s22p4。钠原子的结构示意图为
。氧原子的价电子的电子排布式为2s22p4。钠原子的结构示意图为 。
。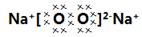 ,其中的阳离子与阴离子的个数比2︰1。
,其中的阳离子与阴离子的个数比2︰1。 2Al2O3+3TiC。
2Al2O3+3TiC。

科目:高中化学 来源:不详 题型:推断题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
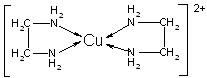
| A.配位键 | B.极性键 | C.离子键 | D.非极性键 |
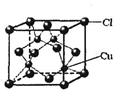
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子间形成的氢键使物质的熔点和沸点升高; |
| B.冰中存在氢键,水中不存在氢键; |
| C.每一个水分子内含有两个氢键; |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 |
| B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C.HI的相对分子质量大于HF,所以HI的沸点高于HF |
| D.由ⅠA族和ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子型化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com