
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.9g 13CO2与N217O的混合物中所含中子数目为4.6NA
B.1L 0.1 mol·L-1 Na2CO3溶液中,CO32-离子数小于0.1NA
C.7.1g Cl2与足量NaOH溶液反应转移的电子数为0.2NA
D.14g乙烯中含有的共用电子对数为3NA
【答案】C
【解析】
A.13CO2与N217O摩尔质量相同,中子数也相同;
B.根据CO32-离子会发生水解进行分析;
C.根据方程式Cl2+2NaOH=NaCl+ NaClO+H2O分析电子转移数量,进一步进行计算;
D.根据乙烯的电子式判断存在的共用电子对数量,进一步进行计算。
A. 13CO2与N217O摩尔质量均为45g/mol,中子数均为23,9g 13CO2与N217O的混合物为0.2mol,中子的物质的量为![]() =4.6mol,中子数目为4.6NA,A项正确;
=4.6mol,中子数目为4.6NA,A项正确;
B. 1L 0.1 mol·L-1 Na2CO3溶液含Na2CO30.1mol,但由于CO32-离子会发生水解,因而CO32-离子数小于0.1NA,B项正确;
C. 根据方程式Cl2+2NaOH=NaCl+ NaClO+H2O可知,消耗1molCl2电子转移1mol,7.1g Cl2是0.1mol,发生反应电子转移0.1mol,那么反应转移的电子数为0.1NA,C项错误;
D.乙烯的分子结构中存在6对共用电子,14g乙烯为0.5mol,含有的共用电子对的物质的量为3mol,故含有的共用电子对数为3NA,D项正确;
答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某课外活动小组设计了下列装置,验证二氧化碳跟过氧化钠反应时需要与水接触。
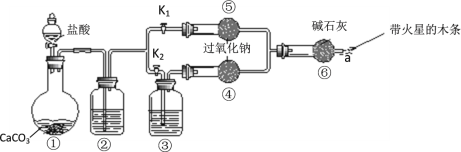
(装置分析)
(1)装置①中反应的离子方程式是___________;
(2)装置②中的试剂是______(填字母),装置③中的试剂是_________(填字母);
a 饱和NaHCO3溶液 b 饱和Na2CO3溶液 c 浓H2SO4 d NaOH溶液
(进行实验)
步骤1:打开弹簧夹K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
(3)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
步骤1中_____________,步骤2中_____________;
(4)步骤2中过氧化钠跟二氧化碳反应的化学方程式是_______________;
(实验反思)
(5)有同学提出质疑:“上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应” 。其理由是____________;
(6)需要补充的实验操作是:取⑤中反应后的少量固体,______________;
(测定实验)测定反应后⑤中固体CO32-的质量分数
(7)将反应后⑤中固体,称量质量为ag。将ag固体溶于水,加入__________(填“BaCl2”或“CaCl2”)溶液,与未选物质相比的优点是___________。将生成的沉淀过滤、洗涤、干燥、称量,得固体质量为bg,计算质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所给信息或标志,判断下列说法错误的是()
A.在实验室和生产生活中,安全都是避免伤害和事故的保障—用肥皂液涂在天然气管道接口处检验是否漏气
B. 在运送硫酸的油罐车上贴有该标志
在运送硫酸的油罐车上贴有该标志
C. 看到有该标志的丢弃物,应远离并报警
看到有该标志的丢弃物,应远离并报警
D. 贴有该标志的物品是可回收物
贴有该标志的物品是可回收物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F均为周期表中前四周期的元素,原子序数依次增大。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体可做半导体材料;F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为________
(2)B的氯化物的熔点比D的氯化物的熔点高的理由是____________。
(3)A的简单氢化物的中心原子采取______杂化,E的低价氧化物分子的空间构型是____。
(4)F的核外电子排布式是_____,A、F形成某种化合物的晶胞结构如图所示(其中A显-3价),则其化学式为_______。
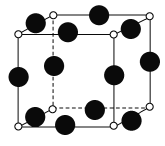
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型锂-空气电池其工作原理如图所示。放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是
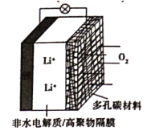
A.锂电极为正极
B.外电路电子由多孔碳材料电极流向锂电极
C.多孔碳材料的O2失电子转化为O2-
D.电池总反应为2Li+(1-x/2)O2=Li2O2-x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.阅读、分析下列两个材料:
材料一
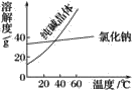
材料二
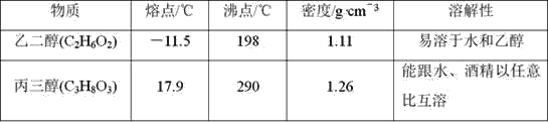
回答下列问题(填字母):
A.蒸馏法 B.萃取法C.“溶解、结晶、过滤”的方法 D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好选用________。
(2)将乙二醇和丙三醇相互分离的最佳方法是________。
Ⅱ.阅读下列材料,按要求回答问题。
酒精、苯、CCl4、煤油都是有机溶剂,有机溶剂之间大都能互溶;碘(I2)难溶于水,易溶于有机溶剂,其溶液呈紫色;溴(液溴)的性质与碘相似,其溶液呈橙色。
(1)下列能用分液漏斗进行分离的是________(填字母)。
A.液溴和CCl4B.酒精和煤油
C.CaCl2和Na2SO4D.苯和蒸馏水
(2)在酒精、苯、CCl4、NaCl、蒸馏水五种试剂中:
①能把碘单质从碘水中萃取出来的是________,进行分液之后________(填“能”或“不能”)得到纯净的碘单质。
②能把溴从溴水中萃取出来,并在分液时溴从分液漏斗下端流出的是________,若观察发现提取Br2以后的水还有颜色,解决该问题的方法是_________________________。
③CCl4能把碘酒中的碘萃取出来吗?________,为什么? ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________。
(2)该溶液中NaOH的质量分数为________。
(3)从该溶液中取出10 mL,含NaOH的质量为________,含NaOH的物质的量为________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物既与硫酸反应,又与氢氧化钠反应的是( )
①NaHCO3 ②NaHSO4 ③(NH4)2CO3 ④NaNO3 ⑤Al(OH)3
A.只有①B.只有③C.①②③D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2O4(g)![]() 2NO2(g) ΔH=+52.70kJ·mol-1
2NO2(g) ΔH=+52.70kJ·mol-1
(1)在恒温、恒容的密闭容器中,进行上述反应时,下列描述中,能说明该反应已达到平衡的是___。
A.v正(N2O4)=2v逆(NO2)
B.容器中气体的平均相对分子质量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
(2)t℃恒温下,在固定容积为2L的密闭容器中充入0.054molN2O4,30秒后达到平衡,测得容器中含n(NO2)=0.06mol,则t℃时反应N2O4(g)![]() 2NO2(g)的平衡常数K=___。若向容器内继续通入少量N2O4,则平衡___移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后NO2的体积分数__原平衡时NO2的体积分数(填“大于”、“小于”或“等于”)。
2NO2(g)的平衡常数K=___。若向容器内继续通入少量N2O4,则平衡___移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后NO2的体积分数__原平衡时NO2的体积分数(填“大于”、“小于”或“等于”)。
(3)取五等份NO2,分别加入到温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g)![]() N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其百分含量随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。
N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其百分含量随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。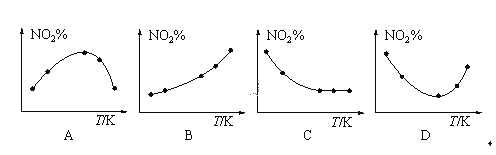
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com