
【题目】下列方程式中,正确的是
A. 0.01mol·L-1NH4Al(SO4)2溶液与0.02mol·L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B. 甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH﹣![]() HCOO﹣+NH4++2Ag↓+3NH3+H2O
HCOO﹣+NH4++2Ag↓+3NH3+H2O
C. 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓
D. 苯酚钠溶液中通入少量CO2:2C6H5O﹣+CO2+H2O→2C6H5OH+CO32﹣
【答案】A
【解析】A.0.01molL-1NH4Al(SO4)2溶液与0.02molL-1Ba(OH)2溶液等体积混合,反应生成硫酸钡、氢氧化铝和一水合氨,反应的离子方程式为NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3H2O,故A正确;B.甲醛和银氨溶液发生银镜反应,原理为:HCHO+4[Ag(NH3)2]++4OH-![]() 4Ag↓+(NH4)2CO3+6NH3+2H2O,故B错误;C.溴乙烷为非电解质,不能电离出溴离子,故C错误;D.苯酚钠溶液中通入少量CO2,反应生成碳酸氢钠,离子方程式:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故D错误;故选A。
4Ag↓+(NH4)2CO3+6NH3+2H2O,故B错误;C.溴乙烷为非电解质,不能电离出溴离子,故C错误;D.苯酚钠溶液中通入少量CO2,反应生成碳酸氢钠,离子方程式:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故D错误;故选A。


科目:高中化学 来源: 题型:
【题目】下列各物质中所含原子个数由大到小的顺序正确的是( )
①0.3molNH3 ②标准状况下22.4L氯气 ③9mL H2O (4℃) ④0.2mol H3PO4
A. ①④③② B. ④③②① C. ②④③① D. ①④②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为同学们使用的一种碳素墨水笔,在组成这种墨水笔的各种材料中:
![]()
(1)属于有机高分子材料的是(选填一种即可)________。
(2)属于金属材料的是(填元素符号)________,______。
(3)目前世界上对废金属材料已得到回收利用,这样做的意义是______。
(4)碳素墨水是________(填“混合物”或“纯净物”)。
(5)写出其中的金属材料与硫酸铜溶液反应的一个化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
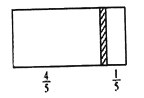
【题目】一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入8molN2,右边充入CO和CO2的混合气体共64g 时,隔板处于如图位置(保持温度不变),下列说法正确的是
A. 右边CO与CO2分子数之比为1:3
B. 右侧CO的质量为14g
C. 右侧气体密度是相同条件下氧气密度的2倍
D. 若改变右边CO和CO2的充入量而使隔板处于距离右端1/3处,保持温度不变,则前后两次充入情况容器内的压强之比为5: 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表得第_____________族,其基态原子中未成对电子的个数为______。
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为____________________,所含非金属元素的电负性由大到小的顺序是____________________。
(3)尿素分子中、碳原子为________杂化,分子中σ键与π键的数目之比为____________________。
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需要知道的数据是______。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为____________________。
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示,则该物质的化学式为____________________。若晶体密度为dg·cm3,则晶胞中最近的两个碳原子的距离为____________________pm(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)3.01×1023个CO2分子中含______mol氧原子,在标准状况下其体积为____L,0.4 molOH-的中有______个电子。
(2)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量为________。
(3)同温同压下,等质量的N2和CO2所含分子数比为_____,体积比为________。
(4)某气体在标准状况下的密度为1.25g/L,则28g该气体所含有的分子数为________。
(5)用98%的浓硫酸(ρ=1.84 g/cm3)配制1 mol/L的稀硫酸l00mL,配制过程中需量取浓硫酸____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)在装置A和装置B中都用到玻璃棒,装置B中玻璃棒的作用是__________,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①的名称是__________,冷却水的方向是__________。装置D在分液时为使液体顺利滴下,应进行的具体操作是__________.
(3)除去自来水中的Cl-等杂质,选择装置__________(填代表装置图的字母,下同)。检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加__________,不产生白色沉淀表明Cl-已除净。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com