
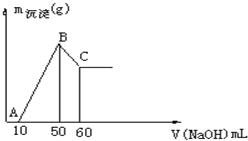
 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.合金中镁铝的物质的量之比为( )
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.合金中镁铝的物质的量之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |


科目:高中化学 来源: 题型:
| A、煅烧石灰石可得生石灰和二氧化碳,该反应是一个放出能量的反应 |
| B、水分解产生氢气和氧气时放出能量 |
| C、相同状况下,反应2SO2+O2═2SO3是一个放热反应,则反应2SO3═2SO2+O2是一个吸热反应 |
| D、氯化氢分解成氢气和氯气时需要吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(1)(4) |
| B、(2)(4) |
| C、(1)(3)(4) |
| D、(1)(2)(3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+和N3-的电子层结构都与氖原子相同 |
| B、Na+的半径大于Na3-的半径 |
| C、Na3N与足量的盐酸反应后生成两种盐 |
| D、在Na3N与水的反应中,Na3N作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、反应速率v正(X)=
| ||
| B、加入X,反应的△H增大 | ||
| C、增加Y的物质的量,X的转化率增大 | ||
D、降低温度,
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol?L-1 的硫酸和0.1mol?L-1 的氢氧化钠溶液 |
| B、0.1mol?L-1 的盐酸和0.1mol?L-1 的氢氧化钡溶液 |
| C、pH=3的醋酸和pH=11的氢氧化钡溶液 |
| D、pH=3的盐酸和pH=11的氢氧化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |
| B、使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾 |
| C、植物油和裂化汽油都可以使溴水褪色 |
| D、神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将FeCl3 溶液滴入蒸馏水中即可 |
| B、将FeCl3 溶液滴入热水中,生成棕黄色液体即可 |
| C、将FeCl3 溶液滴入沸水中,并继续煮沸至生成红褐色液体即可 |
| D、将FeCl3 溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com