
| A、0.1mol?L-1 的硫酸和0.1mol?L-1 的氢氧化钠溶液 |
| B、0.1mol?L-1 的盐酸和0.1mol?L-1 的氢氧化钡溶液 |
| C、pH=3的醋酸和pH=11的氢氧化钡溶液 |
| D、pH=3的盐酸和pH=11的氢氧化钡溶液 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 物质 | 对人类发展的贡献 | 对人类发展带来的问题 | 化学界的解决办法 |
| 硫酸铵等化肥 | 农作物增产数倍,解决了人类的粮食问题 | 造成赤潮、土壤酸化等 问题 | 合理使用化学肥料 |
| 塑料 | 解决包装等材料问题,有效减少了木材和金属等资源的消耗 | 产生了“白色污染” | 研究新型可降解塑料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
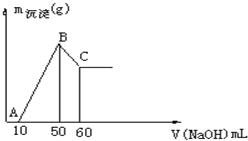 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.合金中镁铝的物质的量之比为( )
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.合金中镁铝的物质的量之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、19.6% | B、22% |
| C、24.9% | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgNO3保存在棕色试剂瓶里 |
| B、Li保存在煤油里 |
| C、用pH试纸测得某盐酸溶液的pH为2.3 |
| D、液溴保存在带橡胶塞的玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在水中加KHCO3 |
| B、在水中加HCl |
| C、在水中加CuCl2 |
| D、将水加热至100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 100mL稀盐酸 |
| NaOH溶液 |
| 100mLNaOH溶液 |
| 稀盐酸 |
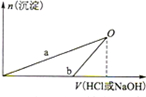 下列说法正确的是( )
下列说法正确的是( )| A、X溶液和Y溶液中均只含一种溶质 |
| B、b曲线表示的是向X溶液中加入NaOH溶液 |
| C、在O点时两方案中所得溶液浓度相等 |
| D、a、b曲线表示的反应都是复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com