
【题目】已知分解1mol H2O2放出热量98kJ,在含少量I- 的溶液中,H2O2分解的机理为①H2O2+I-→H2O+IO-(慢)、② H2O2+IO-→H2O+O2+I-(快)。下列有关该反应的说法不正确的是( )
A.过氧化氢分解快慢决定于反应慢的①
B.![]() 的分解速率与的
的分解速率与的![]() 浓度有关
浓度有关
C.该反应的催化剂是![]() ,而不是
,而不是![]()
D.由于催化剂的加入降低了反应的活化能,也改变了该反应的反应热
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】氧化锌烟灰中主要含有锌、铅、铜、氧、砷、氯等元素。氨法溶浸氧化锌烟灰可制取高纯锌,工艺流程如图所示。
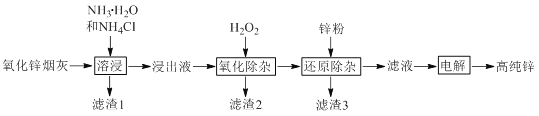
已知氧化锌烟灰经溶浸后,其中的锌、铅、铜、氧、砷元素不同程度的进入浸出液中,其中锌和砷元素分别以Zn(NH3)42+、AsCl52-的形式存在。
回答下列问题:
(1)Zn的原子序数为30,其在元素周期表中的位置为____________。
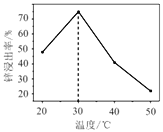
(2)锌浸出率与温度的关系如图所示,分析30℃时锌浸出率最高的原因为______________。
(3)“氧化除杂”中,AsCl52-转化为As2O5胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式__________________________________________。
(4)“滤渣3”除锌外,主要成分为___________________。
(5)“电解”时阳极区放出一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是___________(写名称)。电解后的电解液经补充_________(写一种物质的化学式)后可返回至__________________(填流程中的操作名称)循环利用。
(6)ZnCl2溶液一次水解可获得产物Zn(OH)xCly,取10.64g该水解产物,经二次水解、缎烧后,可得氧化锌8.1g(假设各步均转化完全)。则一次水解产物的化学式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求作答:
(1)有机物命名:
①![]() ______________________________(习惯命名法);
______________________________(习惯命名法);
②(CH3)2CHCH2CH(NH2)COOH_____________________________________(系统命名法)。
(2)书写化学方程式:
①ClCH2CH2COONH4与氢氧化钠的乙醇溶液共热_______________;
②对苯二甲酸(![]() )和乙二醇一定条件下的缩聚反应______________。
)和乙二醇一定条件下的缩聚反应______________。
(3)①某芳香烃的分子式为C8H10,它的一氯代物有二种,则其结构简式为_______;
②环己烷(C6H12)的属于环烷烃的同分异构体,其中含三元环(三角形)的有_______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:

(1)②的元素符号是__________;该元素的最高价氧化物的电子式为__________;
(2)⑤和⑥两种元素的非金属性强弱关系是:⑤________⑥(填“>”或“<”);
(3)①和③两种元素组成的化合物中含有的化学键为__________(填“离子键”或“共价键”)
(4)④和⑥两种元素组成的化合物与AgNO3溶液反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 A、B、C、D、E、F、G 七种元素,试按如下所给的条件推断:
①A、B、C 是同一周期的金属元素,已知原子核外有3个电子层,A 的原子半径在所属周期中最大,且原子半径:A>B>C;
②D、E 是非金属元素,它们与氢化合可生成气态氢化物 HD 和 HE,室温下,D 的单质是液体,E 的单质是固体;
③F是地壳中含量最多的元素,G 是非金属性最强的元素
(1)C 离子的结构示意图为________________________ ;E 单质的颜色为_________。
(2)用电子式表示B、D 元素形成的化合物的形成过程:_____________________________ 。
(3)有 G、F 元素参加的置换反应的化学方程式为___________________________ 。
(4)用离子方程式证明D、E 元素的非金属性强弱,并用单线桥表示电子转移的方向和数目:________________________。
(5)用刺孔的 C单质(足量)包裹住2.3gA 单质放于水中,标准状况下,收集到气体的体积最多为_____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下联氨(N2H4)的水溶液中有:
①N2H4+H2O![]() N2H5++OH- K1
N2H5++OH- K1
②N2H5++H2O![]() N2H62++OH- K2
N2H62++OH- K2
(提示:二元弱碱的电离也是分步电离)
该溶液中的微粒的物质的量分数δ(X)随-lgc(OH-)变化的关系如图所示。下列叙述错误的是( )
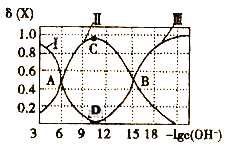
A.据A点可求:K1=10-6
B.D点溶液的c(OH-)=10-l1
C.若C点为N2H5Cl溶液,则存在:c(Cl-)>c(N2H5+)+2c(N2H62+)
D.在N2H5Cl水溶液中,c(N2H4)+c(OH-)=2c(N2H62+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴、 铜及其化合物在工业上有重要用途, 回答下列问题:
(1) 请补充完基态Co的简化电子排布式: [Ar]_________, Co2+有_______个未成对电子。
(2) Na3[Co(NO2)6]常用作检验K+的试剂, 配位体NO2-的中心原子的杂化形式为________, 空间构型为_____。大π键可用符号![]() 表示, 其中m代表参与形成大π键的原子数, n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为
表示, 其中m代表参与形成大π键的原子数, n为各原子的单电子数(形成σ键的电子除外)和得电子数的总和 (如苯分子中的大π键可表示为![]() ),则NO2-中大π键应表示为____________。
),则NO2-中大π键应表示为____________。
(3) 配合物[Cu(En)2]SO4的名称是硫酸二乙二胺合铜(Ⅱ), 是铜的一种重要化合物。其中 En 是乙二胺(H2NCH2CH2NH2)的简写。
①该配合物[Cu(En)2]SO4中N、 O、 Cu的第一电离能由小到大的顺序是______________。
②乙二胺和三甲胺[N(CH3)3]均属于胺, 且相对分子质量相近, 但乙二胺比三甲胺的沸点高得多, 原因是______________________________________________________。

(4) 金属Cu晶体中的原子堆积方式如图所示, 其配位数为______, 铜的原子半径为a nm, 阿伏加德罗常数的值为NA, Cu的密度为_________g/cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积为1 L的密闭容器中,通入一定量的CO和H2O,在850 ℃ 发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。CO和H2O浓度变化如图:
CO2(g)+H2(g) ΔH<0。CO和H2O浓度变化如图:

(1)0~4 min的平均反应速率v(CO)=__________________mol·(L·min)-1。
(2)850 ℃时,平衡常数K=___________________。
(3)850 ℃时,若向该容器中充入1.0 mol CO、3.0 mol H2O,则CO的平衡转化率为___________。
(4)能判断该反应达到化学平衡状态的依据是________(填选项序号)。
a.v正(H2)=v逆(H2O) b.c(CO2)=c(CO)
c.容器中气体密度不变 d.1 mol H—H键断裂的同时断裂2 mol H—O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号,其中J为0族元素。
X | Y | Z | |
R | |||
W | |||
J |
下列说法正确的是( )
A.R原子的核外电子排布图为![]()
B.Y2-与Na+的半径大小关系为Y2->Na+
C.X的第一电离能小于Y的第一电离能
D.表中电负性最大的元素为W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com