
| A、无水硫酸铜、蔗糖 |
| B、食盐、硫酸亚铁 |
| C、硅胶、硫酸亚铁 |
| D、生石灰、食盐 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、某有机物燃烧只生成CO2和H2O,二者物质的量相等,此有机物的组成为CnH2n |
| B、相同物质的量的烃,完全燃烧,生成的CO2越多,说明烃中的碳元素的含量越大 |
| C、某气态烃CxHy与足量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则y=4;若体积减小,则y>4;反之,则y<4 |
| D、相同质量的烃,完全燃烧,消耗O2越多,烃中的氢元素的含量越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7 | B、6 | C、5 | D、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极的电极反应式:O2+4H++4e-=2H2O |
| B、溶液中的阴离子向正极移动 |
| C、溶液的pH值保持不变 |
| D、负极的电极反应式:N2H4+4OH--4e-=4H2O+N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属元素和非金属元素分界线附近 |
| B、过渡元素 |
| C、左下方区域的金属元素 |
| D、右上方区域的非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硒也有两种氧化物,分别为SeO2和SeO3两种 |
| B、硒化氢属于共价化合物,比硫化氢稳定 |
| C、硒化氢的水溶液显弱酸性 |
| D、硒单质的非金属性比氧弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,4.4 g CO2与N2O混合气体中含有的原子总数为0.3NA |
| B、标准状况下,2.24L已烷含有分子的数目为0.1NA |
| C、1 L 1 mol?L-1的CuCl2 溶液中含有Cu2+的数目为NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 酯交换 |

 )结构
)结构查看答案和解析>>
科目:高中化学 来源: 题型:
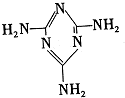 )俗称.蛋白精”,可以由下列反应合成:
)俗称.蛋白精”,可以由下列反应合成:
| ||
| ||
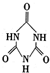 )后,两者之间易通过
)后,两者之间易通过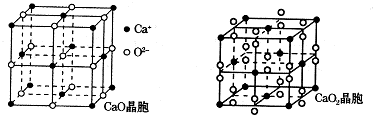
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com