
【题目】对溴苯乙烯(![]() )与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。完成下列填空:
)与丙烯的共聚物是一种高分子阻燃剂,具有低毒、热稳定性好等优点。完成下列填空:
(1)写出该共聚物的结构简式___________。
(2)实验室由乙苯制取对溴苯乙烯,需先经两步反应制得中间体![]() 。写出该两步反应所需的试剂及条件____________,____________。
。写出该两步反应所需的试剂及条件____________,____________。
(3)将![]() 与氢氧化钠溶液共热得到A
与氢氧化钠溶液共热得到A![]() ,写出上述反应的条件___________;由上述反应,关于卤代烃水解反应你可以得到的结论为__________________;写出A生成对溴苯乙烯的反应的化学方程式_______________。
,写出上述反应的条件___________;由上述反应,关于卤代烃水解反应你可以得到的结论为__________________;写出A生成对溴苯乙烯的反应的化学方程式_______________。
(4)以1,3-丁二烯为原料制备工程塑料PB的原料之一的l,4-丁二醇(BDO)的合成路线:C4H6![]() C4H6Cl2
C4H6Cl2![]()
![]() BDO。写出上述由A制备BDO的化学方程式:
BDO。写出上述由A制备BDO的化学方程式:
①反应④________
②反应⑤________
③反应⑥________
【答案】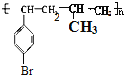 液溴、溴化铁作催化剂 溴、光照 氢氧化钠的水溶液,加热 卤代烃水解时羟基只能取代苯环侧链上的卤原子
液溴、溴化铁作催化剂 溴、光照 氢氧化钠的水溶液,加热 卤代烃水解时羟基只能取代苯环侧链上的卤原子 ![]()
![]()
![]() +H2O CH2=CH﹣CH=CH2+Cl2
+H2O CH2=CH﹣CH=CH2+Cl2![]() CH2Cl﹣CH=CHCH2Cl CH2Cl﹣CH=CHCH2Cl+2NaOH
CH2Cl﹣CH=CHCH2Cl CH2Cl﹣CH=CHCH2Cl+2NaOH![]() CH2OH﹣CH=CHCH2OH+2NaCl CH2OH﹣CH=CHCH2OH+H2
CH2OH﹣CH=CHCH2OH+2NaCl CH2OH﹣CH=CHCH2OH+H2![]() CH2OH﹣CH2CH2CH2OH
CH2OH﹣CH2CH2CH2OH
【解析】
(1)对溴苯乙烯与丙烯在一定条件下发生加聚反应生成高分子化合物,其结构简式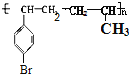 或
或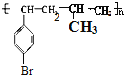 ;
;
(2)乙苯生成![]() 时,苯环上H原子被取代需要溴化铁作催化剂,需要液溴作反应物;支链上H原子被取代需要光照条件,需要溴作反应物;
时,苯环上H原子被取代需要溴化铁作催化剂,需要液溴作反应物;支链上H原子被取代需要光照条件,需要溴作反应物;
(3)该反应为卤代烃的取代反应,反应条件为氢氧化钠的水溶液,加热;苯环上的卤原子没有被取代,说明卤代烃水解时羟基只能取代苯环侧链上的卤原子;![]() 在浓硫酸加热的条件下羟基可以发生消去反应,方程式为
在浓硫酸加热的条件下羟基可以发生消去反应,方程式为![]()
![]()
![]() +H2O;
+H2O;
(4)①BDO为l,4-丁二醇,所以C4H6与氯气发生1,4加成反应生成C4H6Cl2,方程式为CH2=CH-CH=CH2+Cl2![]() CH2Cl-CH=CHCH2Cl;
CH2Cl-CH=CHCH2Cl;
②氯原子在氢氧化水溶液加热的条件下发生取代反应,方程式为:CH2Cl-CH=CHCH2Cl+2NaOH![]() CH2OH-CH=CHCH2OH+2NaCl;
CH2OH-CH=CHCH2OH+2NaCl;
③CH2OH-CH=CHCH2OH与氢气发生加成反应生成BDO,方程式为:CH2OH-CH=CHCH2OH+H2![]() CH2OH-CH2CH2CH2OH。
CH2OH-CH2CH2CH2OH。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在固态金属氧化物电解池中,高温共电解H2O—CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是( )
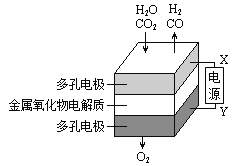
A.阴、阳两极生成的气体的物质的量之比是1︰2
B.X是电源的负极
C.阴极的反应式是:H2O+2e-=H2+O2- CO2+2e-=CO+O2-
D.总反应可表示为:H2O+CO2![]() H2+CO+O2
H2+CO+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高。DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量溶液的pH等而在中和滴定的研究中应用越来越广泛深入。

(1)某学习小组利用DIS系统探究强碱和不同酸的中和反应,实验过程如下:
①分别配制0.1000mol/L的NaOH、HCl、CH3COOH溶液备用。
②用0.1000mol/L的NaOH溶液分别滴定10.00mL0.1000mol/L的HCl和CH3COOH溶液,连接数据采集器和pH传感器。
③由计算机绘制的滴定曲线如图一:
两曲线图起点不同的原因是_____;两曲线图中V1_____V2 (填“>”、“=”或“<”)。
(2)另一个学习小组利用DIS系统测定某醋酸溶液的物质的量浓度,以测量溶液导电能力来判断滴定终点,实验步骤如下:
①用_____(填仪器名称)量取20.00mL醋酸溶液样品,倒入洁净干燥锥形瓶中,连接好DIS系统.如果锥形瓶中含有少蒸馏水,是否会影响测量结果_____(填“是”、“否”、“不能确定”)。向锥形瓶中滴加0.1000mol/L的NaOH溶液,计算机屏幕上显示出溶液导电能力与加入NaOH溶液体积关系的曲线图(见图二)。
②醋酸与NaOH溶液反应的离子方程式为___________________________。
③图中b点时,溶液中各离子浓度大小的关系是_____________________。
④若图中某一点pH等于8,则c(Na+)﹣c(CH3COO﹣)的精确值为_____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是

A.图甲表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
B.图乙是金刚石与石墨分别氧化生成CO2的能量关系曲线,说明石墨转化为金刚石的反应的ΔH>0
C.图丙表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率大于b点
D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学在实验室研究Al与CuCl2溶液的反应.
实验操作 | 实验现象 |
|
|
(1)现象![]() 中的红色物质是 ______ .
中的红色物质是 ______ .
(2)经检验现象![]() 中的无色气体为氢气.
中的无色气体为氢气.
①甲认为Al与H+反应产生了氢气,用离子方程式表示溶液中存在大量H+的原因 ______.
②氢气从红色物质表面逸出的原因是 ______ .
(3)探究白色沉淀的化学成分.
查阅资料:Cu+可与浓氨水反应生成Cu(NH3)2+(无色),该无色物质在空气中易被氧化变为蓝色.
乙认为白色沉淀可能是CuCl,并通过实验证明其猜测正确,实验步骤如下:
a.取白色沉淀,充分洗涤;
b.向其中加入浓氨水,沉淀溶解得到无色溶液,将无色溶液分为两份;
c.取其中一份无色溶液![]()
d.将另一份无色溶液放置于空气中,一段时间后,溶液变为蓝色.
①步骤c的实验方案是 ______.
②用化学平衡移动原理解释CuCl溶于浓氨水的原因 ______.
(4)探究CuCl产生的原因.
①丙猜测可能是Cu与CuCl2溶液反应生成了CuCl,因为Cu具有 ______性.
②取Cu粉与1mol/LCuCl2溶液混合,无白色沉淀产生,丙再次分析Al与CuCl2溶液反应的实验现象,改进实验方案,证明了Cu与CuCl2溶液反应生成了CuCl,改进之处是 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】250C时,向20.0mL0.10mol/L氨水中滴入0.10mol/L盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10mol/L氨水的电离度为1.32%,下列有关叙述不正确的是( )
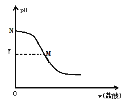
A.本实验应选用的指示剂是甲基橙
B.M点处的溶液中c(NH4+)=c(Cl)>c(H+)=c(OH)
C.N点处的溶液中pH<12
D.M点对应的盐酸体积为20.0mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。
Ⅰ.亚氯酸钠的制备
以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
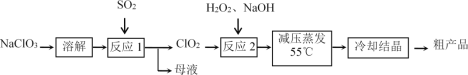
(1)“反应1”中的氧化剂是_____(填化学式,下同),母液中溶质的主要成分是_____。
(2)每有1mol SO2参加反应,理论上可生成ClO2的物质的量为________mol。
(3)如果将SO2换为Na2SO3和稀H2SO4,则“反应1”的离子方程式为________。
(4)“反应2”使用H2O2而不使用其他物质的主要理由是____________________。
Ⅱ.亚氯酸钠的应用
(5)用亚氯酸钠作水处理剂,水中可能残留少量亚氯酸钠,可以加入硫酸亚铁除去残留的亚氯酸盐,硫酸亚铁除可与亚氯酸钠反应外,还可以起到的作用是____________。
(6)实验室可用亚氯酸钠和氯酸钠在酸性条件下反应制备ClO2气体。
①上述反应的离子方程式为____________。
②ClO2也可用于杀菌消毒,其消毒能力是等物质的量Cl2的_______倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁溶液水解可以得到一系列具有净水作用的碱式硫酸铁(xFe2O3ySO3zH2O),为测定某碱式硫酸铁的组成,取5.130g样品溶于足量盐酸中,然后加入过量的BaCl2溶液,经过滤、洗涤、干燥得白色固体5.825g,向上述滤液中加入过量的NaOH溶液,经过滤、洗涤、灼烧得到固体1.600g,该样品的化学式为( )
A.Fe2O32SO37H2OB.4Fe2O310SO325H2O
C.3Fe2O36SO320H2OD.2Fe2O35SO317H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图。下列说法不正确的是

A.该过程中H2O被还原生成氧气
B.该过程中涉及极性键和非极性键的断裂与生成
C.基于合成NH3的过程属于氮的固定
D.该过程的化学方程式为:2N2+6H2O![]() 4NH3+3O2
4NH3+3O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com